Cuprins
- 1. Structura moleculei de apa
- 2. Forte intermoleculare
- 3. Structura apei
- 4. Proprietatile apei
- 5. Disocierea apei
- 6. Puritatea apei
- 7. Tehnici fizice de studiu al apei în sistemele biologice
- 8. Fenomene la nivelul interfetelor
- 9. Cristale lichide
Extras din curs
Apa este cea mai importanta substanta necesara vietii. Datorita structurii si interactiilor sale
moleculare, apa prezinta proprietati unice, de care organismele vii depind într-un mod complex si
ireversibil. Organismele vii contin apa în proportie de cel putin 50%. In mediul extracelular, factorii
nutritivi sunt dizolvati în apa, fapt ce le permite sa traverseze membranele celulare, iar în interiorul
celulelor, mediile în care se desfasoara numeroase reactii chimice sunt medii apoase, care permit de
asemenea aparitia unor fluxuri de substanta în interiorul celulei. La temperatura normala a
organismului, apa se afla în stare lichida, ceea ce îi confera caracterul de complexitate si dinamism,
spre deosebire de starea solida, în care libertatea miscarilor moleculare este extrem de limitata, sau
fata de starea gazoasa, în care gradul de complexitate este redus, datorita dezordinii moleculare
specifice acestei stari.
1. Structura moleculei de apa
Molecula de apa (H2O) este alcatuita din doi atomi de hidrogen si un atom de oxigen. In
molecula izolata de apa, atomul de oxigen formeaza legaturi covalente cu cei doi atomi de hidrogen,
distanta dintre nucleul O si un nucleu H fiind de cca. 0,97 Å, iar unghiul format de cele doua
legaturi O-H este de 104,5º.
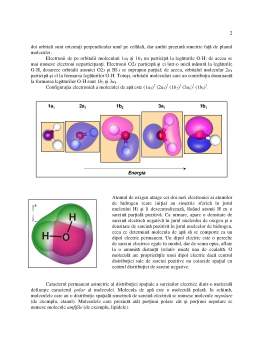
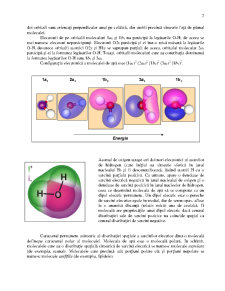
Configuratia electronica a hidrogenului este 1s1, iar cea a oxigenului 1s2 2s2 2p4. Dintre cei 4
electroni de pe patura 2p a oxigenului, doi au spinul compensat si completeaza un orbital atomic, iar
ceilati doi ramân cu spinul necompensat, pe doi orbitali atomici diferiti (Un orbital electronic,
atomic sau molecular, nu poate avea decât cel mult doi electroni, care trebuie sa aiba spinul de semn
opus). Ca urmare, cei 10 electroni ai moleculei de apa se distribuie astfel:
- doi electroni proveniti de pe orbitalul 1s al atomului de oxigen (cel mai apropiat de nucleul O)
completeaza orbitalul molecular 1a1; acest orbital corespunde primului nivel energetic al moleculei
de apa si este sferic, centrat pe nucleul de oxigen;
- doi electroni proveniti de pe orbitalul O2s completeaza orbitalul molecular 2a1; acesta este
aproximativ sferic, centrat pe nucleul de oxigen, dar usor deformat datorita influentei electronilor
H1s;
- doi electroni proveniti de pe orbitalul complet O2p corespund orbitalului molecular 1b1, care este
orientat perpendicular pe planul moleculei; acest orbital nu este deformat de ceilalti electroni;
- ceilalti doi electroni 2p ai oxigenului completeaza, fiecare împreuna cu câte un electron 1s al
hidrogenului, doi orbitali moleculari, 1b2 si 3a1, formând astfel doua legaturi covalente O-H. Acesti
2
doi orbitali sunt orientati perpendicular unul pe celalalt, dar ambii prezinta simetrie fata de planul
moleculei.
Electronii de pe orbitalii moleculari 1a1 si 1b1 nu participa la legaturile O-H; de aceea se
mai numesc electroni neparticipanti. Electronii O2s participa si ei într-o mica masura la legaturile
O-H, deoarece orbitalii atomici O2s si H1s se suprapun partial; de aceea, orbitalul molecular 2a1
participa si el la formarea legaturilor O-H. Totusi, orbitalii moleculari care au contributia dominanta
la formarea legaturilor O-H sunt 1b2 si 3a1.
Configuratia electronica a moleculei de apa este (1a1)2 (2a1)2 (1b2)2 (3a1)2 (1b1)2.
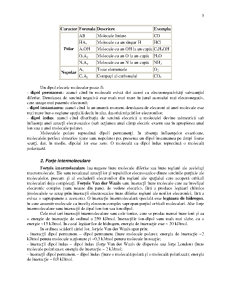
Atomul de oxigen atrage cei doi nori electronici ai atomilor
de hidrogen (care initial au simetrie sferica în jurul
nucleului H) si îi descentralizeaza, lasând atomii H cu o
sarcina partiala pozitiva. Ca urmare, apare o densitate de
sarcina electrica negativa în jurul nucleului de oxigen si o
densitate de sarcina pozitiva în jurul nucleelor de hidrogen,
ceea ce determina molecula de apa sa se comporte ca un
dipol electric permanent. Un dipol electric este o pereche
de sarcini electrice egale în modul, dar de semn opus, aflate
la o anumita distanta (relativ mica) una de cealalta. O
molecula are proprietatile unui dipol electric daca centrul
distributiei sale de sarcini pozitive nu coincide spatial cu
centrul distributiei de sarcini negative.
Preview document
Conținut arhivă zip
- Apa in Sistemele Biologice.pdf