Extras din laborator
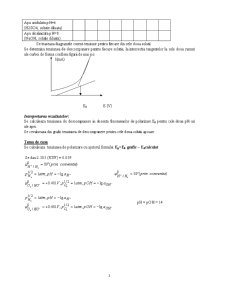
In toate aplicatiile practice cu celule de electrolizei (curatirea si prelucrarea suprafetelor metalice, protectia metalelor prin depuneri galvanice de metale sau straturi de conversie, in electrovopsire) cit si in cele in care intervin celule galvanice (polisare chimica) randamentul procesului de electroliza sau de descarcare este subunitar (respectiv < 100%) datorita fenomenelor de polarizare.
Procesele de polarizare apar cand la interfata metal /solutie de electrolit trece un curent electric: curent de electroliza in celulele de electroliza sau curent de descarcare in celulele galvanice.Trecerea curentului electric modifica valoriea potentialului de electrod. Aceasta schimbare a valorii potentialului de electrod din circuitul deschis la trecerea curentului electric se numeste polarizare. Potentialul electrodului polarizat depinde de valoarea curentului ce trece la interfata metal /solutie.
Fenomenul de polarizare se studiaza analizind mecanismul reactiilor de oxidoreducere ce au loc in absenta si la trecerea curentului electric.
Principiul lucrarii Lucrarea practica se ocupa de fenomenele de polarizare la electroliza apei.
In timpul electrolizei apei, intre anod si catod apare o diferenta de potential de semn contrar tensiunii aplicate din exterior, iar cauza lui este desfasurarea unor reactii secundare la electrozi.
Apa este un electrolit slab care se disociaza potrivit reactiei:
H2O”H+ + OH-
Reactiile care au loc la anod si la catod in celula de electroliza la trecerea curentului electric sunt:
Catod (-): 2H+ + 2e- * H2 si
Anod (+): 2OH- - 2e- * H2O + 1/2 O2
La valori mici ale tensiuni aplicate, hidrogenul si oxigenul care se formeaza in stare de gaz nu se desprind de electrozi. Astfel, la catodul celulei de electroliza se acumuleaza hidrogen molecular in stare de gaz, formand electrodul de hidrogen, iar la anodul celulei de electroliza se acumuleaza oxigen in stare de gaz, formand electrodul de oxigen.
Circuitul fiind inchis, simultan functioneaza si celula de electroliza si in opozitie cu ea (legata in paralel) celula galvanica (-) (Pt) H2 / H+ OH- / O2 (Pt) (+) care determina aparitia fenomenelor de polarizare.
Preview document
Conținut arhivă zip
- Tensiunea de descompunere a apei.doc