Cuprins
- I. Problematica poluarii mediului in cazul procesului studiat
- I.1. Descrierea procesului tehnologic.Scheama bloc.Fluxuri de materiale si energie
- Identificarea surselor si cauzele poluarii
- I.2. Caracterizarea fizico chimica a poluantilor principali
- I.3. Impactul poluantilor asupra mediului
- I.4. Inventarul emisiilor poluante din proces.Bilant cantitativ
- I.5. Reglementari nationale si internationale privind prevenirea poluarii.
- Valori limita de emisie.Concentratia maxima admisa,directiva pentru calitatea mediului
- II. Masuri de prevenire a poluarii pentru procesul studiat
- II.1. Identificarea optiunilor de prevenire a poluarii in conformitate cu cele mai bune tehnici
- disponibile (B.A.T)
- II.2. Selectarea obtiunilor de prevenire a poluarii in vederea alegerii variantei optime
Extras din proiect
1.1 Descrierea procesului tehnologic schema bloc
fluxuri de materiale si energie
Acidul sulfuric, H2SO4, este un foarte activ acid mineral (nu este un acid organic); totodată este cel mai important compus al sulfului. Poate forma orice concentraţie cu apa. Numele vechi al acidului sulfuric este ulei de vitriol sau, după Albert cel Mare însecolul al XIII-lea,ulei de vitriol roman Când sunt adăugate concentraţii mari de trioxid de sulf SO la fabricarea acidului, rezultă o soluţie de SO3 în H2SO4. Aceasta se numeşte
acid sulfuric fumans, oleum, sau acid Nordhausen - H2S2O7
Unul din procedeele de obtinere a acidului sulfuric este arderea piritei. Pirita este un mineral din clasa sulfurilor, cu formula chmică FeS2, de culoare gălbui-arămie cu reflexe verzui și care cristalizează în sistemul cubic.Pirita este colectata din zacaminte si adusa intr-o camera de concasare. De aici ea este trimisa intr-un cuptor de ardere sub actiunea aerului.In urma arderii rezulta SO2, praf si rezidiu solid constituit in special din fier.SO2 este apoi trecut intro camera de desprafuire unde se indeparteaza praful.Urmatoarea etapa este cea de oxidare a SO2 la SO3 intro camera de oxidare.Ultima etapa este cea de absorbtie a SO3 in apa de unde rezilta oleum sau cu o concentratie de 110%.
Reactiile care rezilte in urma procesului de ardere a piritei sunt urmatoarele:
4 FeS2(s) + 11 O2(g) → 2 Fe2O3(s) + 8 SO2(g)
2SO2(g) + O2(g) → 2 SO3(g)
SO3 + H2O → H2SO4 (diluat 5% )
SO3 + H2SO4 → H2SO4 ( concentrate )
S03 + H2SO4 conc → H2SO4 + S03 ( oleum 110% )
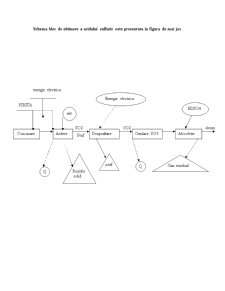
Schema bloc de obtinere a acidului sulfuric este prezentata in figura de mai jos
energie electrica
PIRITA
SO2 SO2 oleum o Praf
Bilanţul de materiale este expresia matematică a acestei legi şi poate fi redat, în general, printr-o relaţie de formă :
ΣMi = ΣMr + ΣMp în care :
ΣMi – masele materiilor prime introduse în sistem
ΣMr - masele produselor rezultate
ΣMp – masele pierderilor
MATERII PRIME:
• Pirita
MATERII AUXILIARE:
• Energie electrica
• Apa
• Aer
REZIDURI:
• Apa uzată (emisie lichidă)
• SO2 (emisie gazoasă)
• Praf
• Rezidiu solid
Identificarea surselor si cauzele poluarii:
Factorii de poluare pot proveni atât în urma procesului tehnologic cât şi datorită condiţiilor de igienizare din unitatea de producţie. Surse şi factori de poluare rezultaţi în urma operaţiilor tehnologice sunt:
1. În cadrul recepţiei, pirita poate contine alte impuritati care in urma introducerii in procesul de fabricatie pot duce la deteriorarea utilajelor.
2. În cadrul arderii piritei rezulta praf si S02 care in urma neglijentei sau a desectiunilor aparute se pot evacua in atmosfera.
3. I cadrul operatiunii de desprafuire trebuie sa existe o camera colectoare de praf pentru a impiedica separarea lui in aer.
Preview document
Conținut arhivă zip
- Prevenirea Poluarii Mediului in Cazul unui Proces de Fabricatie a Acidului Sulfuric din Pirita.doc