Cuprins
- 1. CUPRINS
- 2. GENERALITATI (grupa aVI-a principala) PAG 01
- (oxizii) PAG 03
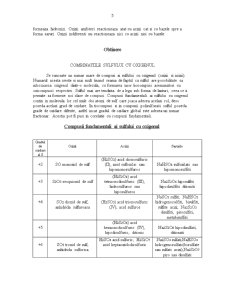
- 3. OBTINERE PAG 04
- 4. EXEMPLE DE OXIZI(structura, proprietati fizice si chimice, utilizari) PAG 05PAG 20
- *Monoxidul de disulf ;
- *Monoxidul de sulf ;
- *Trioxidul de disulf ;
- *Dioxidul de sulf ;
- *Trioxidul de sulf ;
- 5. BIBLIOGRAFIE
Extras din proiect
Generalitati: ”Grupa a VI-a principala. Oxizii sulfului”
*Grupa a VI-a principala*
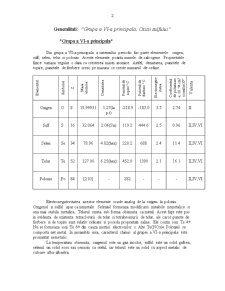
Din grupa a VI-a principala a sistemului periodic fac parte elementele: oxigen, sulf, selen, telur si poloniu. Aceste elemente poarta numele de calcogene. Proprietatile fizice variaza regulat o data cu cresterea masei atomice. Astfel, densitatea, punctele de topire, punctele de fierbere cresc pe masura ce creste numarul de ordine.
Elementul Simbolul Z Masa atomica Densitatea Punctul de topire ° C Punctul de fierbere ° C Electronegtivitatea Coeficientul de polarizare α. 10 ־²4 cm³ a ionilor X²־ Valenta
Oxigen
II,IV,VI
Electronegativitatea acestor elemente scade analog de la oxigen la poloniu. Oxigenul si sulful apar ca nemetale. Seleniul formeaza modificatii instabile nemetalice si una mai stabila metalica. Telurul exista sub forma obisnuita ca metal. Acest fapt este pus in evidenta de existenta tetraclorurii de telur si tetrabromurii de telur, ale caror puncte de fierbere si de topire sunt relativ ridicate si poseda proprietati saline. Ele contin ioni Te 4+. Nu se formeaza ioni Te 6+ din cauza inertiei electronilor s. Alte Te(NO3)4. Poloniul se comporta net metal. In ansamblu insa, caracterul chimic al grupei a VI-a principala este pronuntat nemetalic.
La temperatura obisnuita, oxigenul este un gaz incolor, sulful este un solid galben, selenul un solid rosu sau cenusiu ca otelul, iar telurul este un solid cu aspect metalic de culoare alba-albastra.
Ca toate elementele prime ale grupelor, oxigenul prezinta caractere speciale. El are un rol special prin multimea combinatiilor minerale si organice pe care le formeaza, prin diversele tipuri de lagaturi la care participa, de la legaturi pur ionice la legaturi covalente, prin proprietatile sale paramagnetice, datorita moleculei biradical O2. Oxigenul singur se abate de la regula conform careia numarul grupei corespunde valentei maxime. Oxigenul are un rol considerabil in determinarea structurii unui numar mare de compusi care sunt construiti dintr-o retea de atomi de oxigen in care intra atomii electropozitivi.
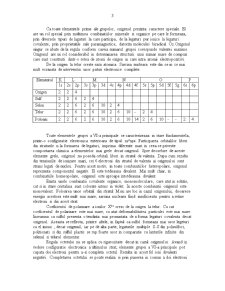
De la oxigen la telur creste raza atomica. Sarcina nucleara este din ce in ce mai mult ecranata de interventia unor paturi electronice complete.
Elementul K L M N O P
1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f 5g 6s 6p
Oxigen 2 2 4
Sulf 2 2 6 2 4
Selen 2 2 6 2 6 10 2 4
Telur 2 2 6 2 6 10 2 6 10 - 2 4
Poloniu 2 2 6 2 6 10 2 6 10 14 2 6 10 - - 2 4
Toate elementele grupei a VI-a principale se caracterizeaza in stare fundamentela, printr-o configuratie electronica exterioara de tipul: ns²np4. Participarea orbitalilor liberi din straturile n la formarea de legaturi, imprima diferente mari in ceea ce priveste comportarea chimica a elementelor mai grele decat oxigenul. Spre deosebire de aceste elemente grele, oxigenul nu poseda orbitali liberi in stratul de valenta. Dupa cum rezulta din tensiunile de ionizare mari, cei 6 electroni din stratul de valenta ai oxigenului sunt strans legati de nucleu. Pentru acest motiv, in toate combinatiilor heteropolare, oxigenul reprezenta componentul negativ. El este totdeauna divalent. Mai mult chiar, in combinatiile homeopolare, oxigenul este aproape intotdeauna divalent.
Exista unele combinatii covalente organice, monomoleculare, care atat in solutie, cat si in stare cristalina sunt colorate intens in violet. In aceste combinatii oxigenul este monovalent. Folosirea unor orbitali din stratul M nu are loc in cazul oxigenului, deoarece energia acestora este mult mai mare, sarcina nucleara fiind insuficienta pentru a retine electroni si din acest strat.
Coeficientii de polarizare a ionilor X²־ cresc de la oxigen la telur. Cu cat coeficientul de polarizare este mai mare, cu atat deformabilitatea particulei este mai mare. Inseamna ca sulful prezenta o tendinta mai pronuntata de a forma legaturi covalenta decat oxigenul. Aceasta se reflecta, printre altele, in faptul ca sulful formeaza mai usor legeturi cu el insusi , decat oxigenul, iar pe de alta parte, legaturile multiple S-S din polisulfori, politionati si din sulful plastic se rup foarte usor in comparatie cu lanturile infinite din selenul si telurul elementar.
Regula octetului nu se aplica cu rigurozitate decat in cazul oxigenului. Avand in vedere configuratie electronica a ultimului strat, elemente grupei a VI-a principale pot capata doi electroni pentru a-si completa octetul. Rezulta in acest fel ioni divalenti negativi. Completarea octetului se poate realiza si prin punerea in comun a doi electroni cu un alt atom, formandu-se doua legaturi covalente normale. Legaturile simple covalente formate cu radicali sau atomi monovalenti sunt unghiulari. Strereochimia acestor compusi deriva din principiul dirijarii valentelor. Aceasta structura imprima compusilor respectivi un moment de dipol.
Cu cresterea volumului atomic, tensiunile de polarizare si potentialele de ionizare scad si o data cu ele scade caldura de formare a hidrurilor gazoase. Pentru apa aceasta este -68.3 kcal, pentru hidogenul sulfurat 4.8 kcal, pentru H2Se 18.5 kcal si pentru H2Te 34.2 kcal.
Seria derivatilor halogenati dicovalenti ai acestor elemente este foarte incompleta(OF2, OCl2, OBr2, SCl2, TeBr2 ,TeI2). Se constata ca distantele intermoleculare din acesti compusi concorda cu cele prevazute pentru o legatura simpla. Abaterea de la ortogonalitate a legaturilor prin oribitali p din compusii MX2 se explica in primul rand prin repulsia intre halogeni.
Preview document
Conținut arhivă zip
- Oxizii Sulfului
- Oxizi sulfului.doc
- Oxizi sulfului.ppt