Cuprins
- CAP I. ACIDUL OXALIC ŞI OXALAŢII
- I.1 GENERALITẢŢI pag. 3-5
- I.2 SURSE (PREZENŢA ÎN ALIMENTE) pag. 6-9
- I.3 TOXICITATE pag. 10
- I.4 EFECTELE GENERATE DE ACIDUL OXALIC ASUPRA CONSUMATORILOR ŞI MǍSURILE DE PROTECŢIE LUATE DE CONSUMATORI pag. 10-12
- I.5 DETERMINAREA ŞI IDENTIFICAREA ACIDULUI OXALIC ŞI A SĂRURILOR SALE ALCALINE pag. 13-28
- BIBLIOGRAFIE pag. 29
Extras din referat
CAP I. ACIDUL OXALIC ŞI OXALAŢII
I.1 GENERALITĂŢI
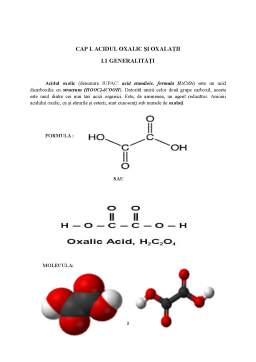
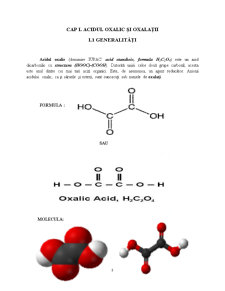
Acidul oxalic (denumire IUPAC: acid etandioic, formula H2C2O4) este un acid dicarboxilic cu structura (HOOC)-(COOH). Datorită unirii celor două grupe carboxil, acesta este unul dintre cei mai tari acizi organici. Este, de asemenea, un agent reducător. Anionii acidului oxalic, ca şi sărurile şi esterii, sunt cunoscuţi sub numele de oxalaţi.
FORMULA :
SAU
MOLECULA:
TABELUL 1. PROPRIETĂŢILE FIZICO-CHIMICE ALE ACIDULUI OXALIC
Denumire chimică acid etandioic OC(=O)C(O)=O
acid etandioic
Formulă chimică C2H2O4
Masă moleculară 90,03 g/mol 90,03 g/mol 90,03 g/mol 90,03 g/mol
Număr CAS [144-62-7]
Densitate 1,77 g/cm3
Punct de fierbere 157 °C subl.
pKa 1,27
4,27
Scriere simplificată OC(=O)C(O)=O
„Dăunător sănătăţii”
R- şi S-text R: 21/22
S: (2-)24/25
MAK 1 mg•m−3
Dacă nu sunt alte indicaţii atunci
se ţine cont de prevederile Standard.
Acidul oxalic are caracter reducător, după cum se vede din reacţia cu oxigenul atomic.
, în prezenţă de KMnO4 în H2SO4;
, în prezenţă de H2SO4.
Acid oxalic a fost descoperit de Scheele, în 1776. În plante ( rubarbă, Rumex acetosa, Oxalis acetosella, Phytolacca, belladonna, etc, conţin acid sau oxalat de potasiu) se gǎseşte, în general în asociere cu calciu sau potasiu. Rubarba conţine, de asemenea oxalat de calciu, la fel ca şi multe alte specii de licheni ,în corpul uman aceasta formeazǎ calculi duri, care sunt forme frecvente de pietre. În combinaţie cu calciu este găsit în ghimbir, rădăcină de orris, valeriana, curcuma, quassia, şi alte medicamente. Ca oxalat de amoniu este prezent în anumite îngrăşăminte.În Cicer arietinum sau năut apare în stare liberă.
Acidul oxalic poate fi, de asemenea, format în mod artificial prin acţiunea acidul azotic în zahăr, melasă, orez, amidon, gumă, lână, mătase, şi mulţi alţi compuşi organici, care se gǎsesc în stare liberǎ. Berthelot l-a obţinut sintetic din acetilena, etilena, propilena, prin oxidare cu permanganat de potasiu.
Acidul oxalic se prezintǎ sub formǎ de cristale prismatice incolore, transparente, oblice. Cristalele sunt inodore şi au un gust puternic acid ,în atmosferă uscată, hârtia de turnesol se înroşește, fără a se înnegri dacǎ cristalele sunt pure şi sunt volatilizate de cǎtre cǎldurǎ. Acidul oxalic se dizolvă: în 8 - 11 părţi de apă la 15.5 ° C (60 ° F), în propria lor greutate de apă la 100 ° C. (212 ° F) şi, în 4 parti de alcool; adǎugând o cantitate mică de acid azotic în apă acesta se dizolvǎ mai uşor.
Aproape toate oxalaţii sunt insolubili în apă, cu excepţia celor alcalini. Oxalatul de calciu este insolubil şi, prin urmare, acidul oxalic este util ca test pentru calciu, şi se gǎseşte de obicei sub formǎ de oxalat de amoniu, dacă băuturile alcoolice care urmează să fie examinat conţin acid liber, aceasta trebuie să fie neutralizat primul, pentru cǎ oxalatul poate detecta calciul doar în fluidele neutre sau alcaline. Acid oxalic redus cu hidrogen este transformat în acid glicolic şi acid acetic, şi dacă acţiunea trebuie să suficient de lungă pantru ca acidul glicolic format sǎ devinǎ în totalitate acid acetic.
Acidul oxalic poate fi detectat în oricare soluţie, fiind în întregime volatilizat de căldură; obţinându-se un precipitat alb cu azotat de argint, solubil în acid azotic şi un precipitat alb cu apă de var, care este insolubil în apă şi acid acetic, dar uşor solubil în acid azotic, şi care, atunci când e uscat şi încălzit, este transformat în carbonat de calciu. Soluţia de sulfat de calciu împreunǎ cu acidul oxalic produce un precipitat alb-albastrui. Acidul oxalic este uneori contaminat cu acid azotic, care ii imprimǎ un miros slab,ducând la apariţia unor pete galbene care plutesc în sticla în care este păstrat acesta. Dacă o soluţie foarte diluată de sulfat de indigo, conţine cristale impure, de acid azotic acesta va decolora soluţia. Pe seama asemănǎrii dintre cristalele acidului oxalic şi ale sulfatului de magneziu, acesta din urmă a fost folosit ca un corp străin. Această asemănare, a condus la numeroase cazuri de intoxicaţie, oamenii confundȃnd acidul cu anumite săruri(Epsom).
Acidul oxalic poate fi de asemenea folosit pentru îndepărtarea petelor de fier-rugină şi a celor de cerneală precum şi ca agent de albire.
Metode de preparare a acidului oxalic
Preview document
Conținut arhivă zip
- Acidul Oxalic si Oxalatii.doc