Extras din referat
Polimeri ai borului
Chimia polimerilor borului reprezinta un capitol nou, in rapida dezvoltare cercetarile desfasurate in acest dimeniu au condus la obtinerea unor noi compusi heteroatomici, caracterizati printr-o mare termorezistenta, deoarece borul formeaza legaturi foarte stabile din punct de vedere termodinamic cu elementele: oxigen, carbon, azot si fosfor.
Combinatiile borului cu hidrogenul
Boranii au constituit obiectul a numeroase cercetari, iar in ultimul timp au fost descoperite noi hidruri. Majoritatea boranilor care au fost complet caracterizati apartin fie seriei BnHn+4, fie seriei BnHn+6 Nomenclatura actuala foloseste prefixele di-, tetra-, penta-, hexaboranpentru a indica numarul atomilor de bor, urmat de un numeral pentru a arata numarul atomilor de hidrogen. De exemplu B5H11 se scrie pentaboran-11.
Boranii superiori se obtin prin incalzirea B2H6 singur sau in curent de hidrogen cand au loc reactii reversibile, asemanatoare cu reactiile de cracare din chimia hidrocarburilor, numai ca au loc la tem mai joase si in absenta catalizatorilor. Studiile cinetice presupun un mecanism radicalic, ca intermediar BH3 La temperaturi ridicate, peste 200oC, boranii dau produse nevolatile, (BH)n, de compozitie variabila care peste 700 oC se descompun in bor si hidrogen.
Determinarea structurii boranilor a prezentat un interes deosebit. Astfel s-a stabilit, prin difractie de neutroni, spectre Raman, spectre IR, difractie de electroni ca in B2H6 , exista doua legaturi de hidrogen in punte, perpendiculare pe planul format din cei doi atomi de bor si ceilalti 4 atomi de hidrogen.
Aceste doua punti de hidrogen sunt punti anormale, se foloseste conceptia legaturilor bielectronice tricentrice, formate prin acoperirea orbitalilor hibrizi sp3 ai borului cu orbitalul 1s al hidrogenului, realizandu-se orbitali moleculari.
Heterocicli ce contin B si N
Heterociclicii ce contin Bsi N au fost mult cercetati in ultimii ani cu toate ca primul compus, borazina a fost preparat in 1926 de Stock si Pohland.
Astazi se cunosc atat cicluri in care alterneaza atomii de B cu N, cat si heterocicli ce contin legaturi B-B sau N-N.
Borul formeaza si compusi ciclici de tip aminoborine conducand la polimeri de coordinatie.
Dintre aceste cicluri, compusul cel mai mult studiat a fost ciclotriborazanul H3B3N3H3, care este numit astazi borazina.
a. borazina nesubstituita a fost preparata prima data prin descompunerea termica, la 200oC, a unui amestec de B2H6 si amoniac sau a compusului de aditie B2H6*2NH3 respectiv (BH3BH2NH3)+(BH4)-:
3 B2H6*2NH3 2(HBNH)3 +12H2
Mecanismul acestei reactii consta in transformari ce trec prin treptele de ”etan anorganic”, „etilena”, si „acetilena” monomere, care in final prin polimerizare ajung la trimerul ciclic:
B2H6 NH3 H3B-+NH3 -H2 H2B- N+H2 HB- N+H (HBNH)3
Borazina se mai poate obtine si prin piroliza altor aducti cu amoniac ai pentaboranului-11, pentabora-9 sau pentaboran-10.
b. G.W. Schaeffer recomanda reactia dintre NH4Cl si MBH4 la 300oC (unde M=Li, Na)
3NH4Cl + 3 MBH4 (HBNH)3 +9H2 + 3MCl
Mecanismul acestei reactii poate fi interpretat in doua moduri:
- Fie prin formarea in prealabil a NH3 si BH3:
6NH4Cl 6NH3 + 6 HCl
6HCl + 6LiBH4 3B2H6+6LiCl + 6H2
6NH3 + 3B2H6+ 2(HBNH)3 + 12 H2
- Fie prin formarea intermediara a NH4(BH4) si descompunerea termica
3LiBH4 + 3NH4Cl NH4(BH4)
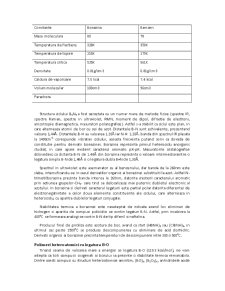
Borazina se prezinta sub forma unui lichid incolor, cu mros aromtic. In tabelul de mai jos se dau unele constante fizice comparabil cu ale benzenului.
Constante Borazina Benzen
Masa moleculara 80 78
Temperatura de fierbere 328K 358K
Temperatura de topire 215K 279K
Temperatura critica 525K 561K
Densitate 0.81g/cm3 0.81g/cm3
Caldura de vaporizare 7.0 kcal 7.4 kcal
Volum molecular 100cm3 96cm3
Parachora
Structura ciclului B3N3 a fost cercetata cu un numar mare de metode fizice (spectre IR, spectre Raman, spectre in ultraviolet, RMN, moment de dipol, difractie de electroni, anizotropie diamagnetica, masuratori polarografice). Astfel s-a stabilit ca ciclul este plan, in care alterneaza atomii de bor cu cei de azot. Distantele B-N sunt echivalente, prezentand valoare 1,44Å. Distantele B-H au valoarea 1.20Å iar N-H 1.20Å. banda din spectrul IR plasata la 1400cm-1 corespunde vibratiei ciclului, aceasta frecventa putand servi ca dovada de constitutie pentru derivatii boeazinei. Borazina reprezinta primul heterociclu anorganic studiat, in care apare evident caracterul aromatic pπ-pπ. Masuratorile cristalografice ddovedesc ca distanta B-N de 1.44Å din borazina reprezinta o valoare intermediaraintre o legatura simpla B-N de 1,48Å si o legatura dubla B=N de 1,30Å.
Preview document
Conținut arhivă zip
- Polimeri Heterociclici Anorganici.doc