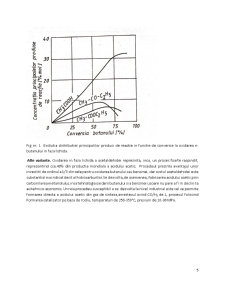
Extras din curs
In acest capitol se prezinta numeroase procese deoxidare partiala a hidrocarburilor, care au loc fie prin introducerea de oxigen in molecula, fie prin reactii de amonoxidare.
BAZELE TEORETICE ALE PROCESELOR DE OXIDARE A HIDROCARBURILOR
1.Termodinamica
Rectiile de oxidare sunt exoterme. Entalpia de oxidare depinde de gradul de oxidare a hidrocarburilor.
CH4 + 1/2O2↔ CH3-OH ΔH298o(kJ/mol)=-128,1 ΔG298o(kJ/mol)=-112,6 lg K298= 19,7
C2H4 + 1/2O2 ↔ CH3 – CHO ΔH298o (kJ/mol)= -218,5 ΔG298o(kJ/mol)=-199,7 lg K298=35,1
Valoarea entalpiei libere de reactie, ΔGo, este adesea apropiata de entalpia de reactie, ΔHo, deoarece termenul TΔS are valori reduse, datorita variatiei mici a entropiei de reactie. Pentru valori negative mari ale entalpiei libere de reactie rezulta, din relatia ΔGo= -RTlnKp,ca valoarea constantei de echilibru va fi foarte ridicata, putindu-se considera, practic, ca reactiile de oxidare, cu introducere de oxigen in molecula hidrocarburii, sunt ireversibile.
Deoarece toate reactiile de oxidare cu oxigen conduc si la formarea de produsi secundari, in practica, in numeroase cazuri, entalpia de reactie este mult mai mare decit cea calculata pe baza ecuatiei stoechiometrice. Agentii cei mai folositi in industrie sunt: oxigenul molecular (aer, sau oxigen tehnic), acidul azotic, oxizii de azot, peroxizii. Natura agentilor oxidanti influenteaza atit entalpia de reactie, cit si distributia produsilor de reactie.
2. Mecanisme si cinetica
Reactiile de oxidare a hidrocarburilor pot decurge in mediu omogen, , necatalitic sau catalitic, in faza lichida sau gazoasa, sau in mediu eterogen, in functie de structura hidrocarburii si de compozitia produsilor dereactie urmariti. Oxidarile care au loc in mediu omogen, la atomii de carbon saturati, decurg, in general, prin mecanism radicalic. Stabilitatea hiroperoxizilor depinde de structura acestora, cei tertiari avand o stabilitate mai buna, ceea ce permite uneori separarea lor in concentratii ridicate (hidroperoxidul de cumen, hidroperoxidul de tert-butil, etc.).Formarea hidroperoxizilor tertiari decurge mai usor, deoarece energia de legatura a hidrogenului cu un carbon tertiar este mai mica: pentru carbonul tertiar este de 372 kJ/mol, pentru carbon secundar este de 393 kJ/mol, iar pentru cel primar, de 410 kJ/mol. Pentru legatura hidrogen-carbon alilic valoarea este de 322 kJ/mol. Usurinta de extragere a hidrogenului este in rapot invers cu energia de legatura. Stabilitatea hidroperoxizilor formati scade cu cresterea temperaturii de oxidare. Initierea reactiilor radicalice se poate realiza termic, cu initiatori sau catalitic. Ultimele variante sunt aplicate cel mai frecvent in industrie.
-oxidari necatalitice
initiere: RH + O2 ---> R˙ +˙OOH
Initiator ---> R˙
propagare: R˙ + O2 ---> ROO˙
ROO˙ + RH --->ROOH + R˙
ROOH ---> RO˙ + ˙OH
RO˙ + RH ---> ROH + R˙
˙OH + RH ---> H2O + R˙
incheiere: Radicali ---> Specii moleculare
Initiatorii se caracterizeaza prin labilitatea lor la temperatura de reactie, putind ceda usor radicali liberi care amorseaza reactia (peroxizi, hidroperoxizi,azoderivati). Propagarea poate conduce la formarea unui numar mare de specii radicalice, care complica compozitia produsilor de reactie. Dintre reactiile radicalice mentionate mai inainte, cea de descompunere a hidroperoxizilor este cea mai prolifica pentru formarea diferitelor specii radicalice si moleculare.
- oxidari catalitice
Reactiile catalitice in mediu omogen implica dispersarea moleculara a catalizatorului in mediul de reactie. In cazul reactiilor omogene in faza gzoasa s-a constatat ca unii compusi halogenati, ca de exemplu HBr, pot fi intrebuintati pentru generarea usoara a radicalilor liberi:
Preview document
Conținut arhivă zip
- Oxidari, Polimerizare, Policondensare.docx