Extras din curs
Cursul 1:
GENERALITATI
Stiinta materialelor defineste legile si furnizeaza mijloacele necesare pentru
a proiecta si realiza diferite categorii de materiale, cu anumite functii de utilizare.
Materialele sunt sisteme solide, care se definesc prin agregate de atomi
(molecule sau ioni) în care fortele de interactiune sunt mai importante decât
agitatia termica. Între particule (atomi, ioni, molecule) se stabilesc anumite
raporturi datorita modificarii straturilor de electroni, cu formarea legaturilor
chimice.
Materialele, la modul general, pot fi clasificate în: materiale naturale (roci,
lemn, minerale diverse) sau transformate chimic (fibre celulozice, cauciuc natural,
carbon) si materiale sintetice (metale, ceramci, sticle, materiale plastice),
elaborate de inginerul de specialitate.
Compozitia chimica a unui material este deci de cele mai multe ori, primul
criteriu cu ajutorul caruia se pot prevede anumite proprietati specifice. Rolul
impuritatilor nu trebuie neglijat, modificari nesemnificative de compozitie putând sa
amelioreze sensibil anumite proprietati sau, din contra, sa conduca la
comportamente speciale care nu sunt tocmai benefice.
Un alt concept de baza care nu trebuie pierdut din vedere este ca exista un
numar mare de corelatii între cele trei notiuni fundamentale, care sunt: modul de
obtinere (sau geneza), compozitia materialului si proprietatile sale, care determina
functia de utilizare a acestor materiale.
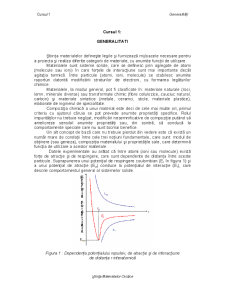
Datele experimentale au aratat ca între atomi (ioni sau molecule) exista
forte de atractie si de respingere, care sunt dependente de distanta între aceste
particule. Suprapunerea unui potential de respingere coulombian (Er în figura 1) si
a unui potential de atractie (Ea) conduce la potentialul de interactie (Ei), care
descrie comportamentul general al sistemelor solide.
Figura 1 : Dependenta potentialului repulsiv, de atractie si de interactiune
de distanta r interatomica
Curs 1 Generalitati
Stiinta Materialelor Oxidice 2
Diagrama pune în evidenta existenta unei distante ro între spatiile dintre
atomi, ioni sau molecule, pentru care valoarea potentialului de interactie este
minima si fortele de respingere si de atractie sunt în echilibru.
Pentru distante r>ro sunt mult mai importante fortele de atractie, iar pentru
distante r<ro sunt mai importante fortele de respingere.
O interactiune este cu atât mai puternica, cu cât distanta de echilibru este
mai mica si nivelul energetic Emin este mai scazut.
Afinitatea pentru electroni a elementelor chimice este definita prin
electronegativitatea acestora. Electronegativitatea, determinata de Pauling,
variaza între 0,7 pentru cesiu si 4,0 pentru fluor.
Tabelul 1: Electronegativitatea elementelor
H
2,1
Li Be B C N O F
1,0 1,5 2,0 2,5 3,0 3,5 4,0
Na Mg Al Si P S Cl
0,9 1,2 1,5
1,8 2,1 2,5 3,0
K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br
0,8 1,0 1,3 1,5 1,6 1,6 1,5 1,8 1,9 1,9 1,9 1,6 1,8 1,8 2,0 2,4 2,8
Rb Sr Y Zr Nb Mo Te Ru Rh Pd Ag Cd In Sn Sb Te I
0,8 1,0 1,2 1,4 1,6 1,8 1,9 2,2 2,2 2,2 1,9 1,7 1,7 1,8 1,9 2,1 2,5
Cs Ba La Hf Ta W Re Os Ir Pt Au Hg Tl Pg Bi Po At
0,7 0,9 1,0 1,3 1,5 1,7 1,9 2,2 2,2 2,2 2,4 1,9 1,8 1,9 1,9 2,0 2,2
Lu
1,2
Fr Ra Ac Th Pa U Np - No
0,7 0,9 1,1 1,3 1,4 1,4 1,4 1,3
Figura 2 reprezinta variatia electronegativitatii în functie de numarul atomic.
Figura 2: Variatia electronegativitatii în functie de numarul atomic
Curs 1 Generalitati
Stiinta Materialelor Oxidice 3
Legaturile chimice între elemente se stabilesc prin interactia straturilor lor de
electroni si, în functie de diferenta între electronegativitatea lor si valoarea
electronegativitatii, pot fi ionice (prin transfer de electroni), covalente (prin punerea în
comun de electroni) si metalice (prin punerea în comun de electroni între toti atomii).
În afara acestor legaturi primare, în corpurile solide se manifesta legaturi
secundare, slabe, rezultate din atractia dipolilor existenti, legaturi cunoscute ca
forte Van der Waals si de asemenea legaturi prin punti de hidrogen. Aceste
interactiuni conduc uneori la proprietati specifice.
Preview document
Conținut arhivă zip
- Stiinta Materialelor Oxice
- 1-Generalitati.pdf
- 10-Biomateriale.pdf
- 11-Dielectrici ceramici.pdf
- 12-lianti.pdf
- 13-nanomateriale.pdf
- 2-aspecte cristalografice.pdf
- 3-defecte.pdf
- 5-structuri silicati.pdf
- 6-structuri oxidice si neoxidice.pdf
- 7-Diagrame binare.pdf
- 8-Diagrame ternare.pdf
- 9-Diagrame aplicate.pdf