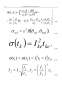Extras din curs
TEORIA LUI BOHR
Informatii pretioase despre electoni se pot obtine din studiile stucturii atomilor .Asa dupa cum s-a aratat în lucrarea :Lumina-unda sau corpuscul? p.228 , pentru expilcarea experientei de împrastiere a razelor ±, Ernest Rutherford (1871-1937) a propus asa numitul model nuclear al atomului .În conformitate cu acest model, un atom este compus dintr-un nucleu încarcat cu un numar de sarcini elementare positive si un numar egal de electroni care graviteaza în jurul acestuia.
Acest model ,att de simplu în aparenta , ridica o problema de importanta exceptionala.
În conformitate cu legile electrodinamicii clasice , o sarcina electrica(în paticular ,un electron), care nu are o miscare rectilinie si uniforma , radiaza unde electromagnetice. Rezulta ca eletronii dintr-un atom , prin miscarea lor în jurul nucleului radiaza unde electromagnetice .Undele electromagnetice radiate preiau o anumita catitate de energie , care este evident suportata de elctronii emitatori. Ca urmare a pierderilor de energie , electronii trebuie sa se roteasca pe niste spirale din ce în ce mai apropiate de nucleu , pna cnd , în final , cad pe el.
Potrivit legilor electrodinamicii clasice, procesul de "cadere" a unui electron pe nucleu dureaza 10 ¾8s. Legile fizicii clasice condamna deci la o moarte sigura" atomul nuclear" .
În realitate, numeroase experiente aratau ca atomii reprezinta niste sisteme stabile, daca, sunt ferite de actiunea unor factori pertubatori externi , au existenta infinita.
Rutherford era constient de soarta pe care i-o oferea fizica clasica atomului pe care el l-a propus. N-a avut alta alternativa , deoarece experientele de împrastiere a particulelor ± aratau cu certitudine existenta î n interiorul atomului a unui nucleu greu pozitiv.
Modelul nuclear sau , cum i se mai spune , modelul planetar – deoarece sructura sa este asemanatoare cu cea a sistemului planetar -, a fost propus de Rutherford în anul 1911 .
Doi ani mai trziu, adica în1913, Niels Bohr (1885 -1962) reuseste , pe baza unor postulate care îi poarta numele, sa calculeze frecventele liniilor spectale emise de cel mai simplu atom – atomul de hidrogen . Postulatele lui Bohr sunt:
1. Atomul este caracterizat prin anumite stari denumit e stari stationare , în care nu emite energie , chiar daca particulele încarcate din atomi au o asfel de miscare înct , dup· legile electrodinamicii clasice , ar trebui sa radieze unde electromagnetice.
2. Orice emisie sau absortie de radiatie electromagnetica corespunde unei treceri dintr-o stare stationara întra-alta, trecere care se numeste tranzitie. La o tranzitie se emite sau se absoarbe un foton a carui frecventa se determina din relatia:
Preview document
Conținut arhivă zip
- BAZE ELTH..doc