Extras din curs
CAPITOLUL I
INTRODUCERE
Termodinamica reprezintă acea parte a fizicii macroscopice care se
ocupă cu studiul relaţiilor dintre fenomenele termice şi cele netermice
(mecanice, elecromagnetice, etc.), fenomene care intervin în caracterizarea
stărilor sistemelor fizico-chimice şi a transformărilor lor.
În terminologia curentă, prin termodinamică se înţelege ştiinţa despre
energie în sensul cel mai larg al cuvântului. Din punct de vedere al
domeniului de utilizare, termodinamica se împarte în trei mari capitole:
termodinamica tehnică (termotehnică) termodinamica chimică şi
termodinamica fizică.
Termotehnica se ocupă cu studiul proceselor ce se desfăşoară în
maşinile şi în instalaţiile termice, procese în care transferul de energie între
corpuri se face sub formă de căldură şi lucru mecanic.
1.1. SISTEMUL TERMODINAMIC
Numim sistem termodinamic un sistem fizico-chimic în care se
delimitează un spaţiu sau o cantitate de materie pentru a studia proprietăţile
termice sau condiţiile de echilibru energetic. Delimitarea sistemului se face
prin suprafeţe de control (reale sau imaginare). Ansamblul corpurilor
înconjurătoare rămase în afara sistemului se numeşte mediu ambiant.
Exemple: un sistem termodinamic poate fi reprezentat de cilindrul unei
maşini termice, cu posibilitatea de a studia proprietăţile gazelor din cilindrul
acelei maşini cu piston.
Un sistem termodinamic poate fi constituit şi din întreaga maşină.
Sistemul în ansamblul său poate schimba energie cu mediul exterior, în
termotehnică interesând schimbul de energie sub formă de căldură şi lucru
mecanic între sistemul termodinamic studiat şi M.E.
După proprietăţile graniţelor sistemului se disting tipurile de sisteme:
- sistem închis (izolat şi neizolat);
- sistem deschis.
Un sistem se numeşte închis dacă nu are schimb de substanţă cu M.E.
(deci conţine întotdeauna aceeaşi cantitate de materie). Un exemplu de
sistem termodinamic închis îl constituie un volum de gaz aflat într-un
cilindru în care se deplasează etanş şi fără frecare un piston.
Prin sistem izolat se înţelege un sistem termodinamic căruia îi este
interzis schimbul de energie cu M.E. (ex: nu este posibilă efectuarea de
- 5 -
lucru mecanic prin deplasarea pistonului, iar pereţii cilindrului nu permit
schimbul de căldură gaz - M.E.).
Un sistem este izolat adiabatic dacă între acesta şi M.E. se realizează
numai schimb de energie sub formă de lucru mecanic, dar schimbul de
căldură nu este permis.
Sistemul din figură este închis dar neizolat, deoarece, prin deplasarea
pistonului are loc un schimb energetic (lucru mecanic).
Figura 1.1
Sistem închis. Gaz închis într-un cilindru prevăzut
cu piston etanş şi fără frecare
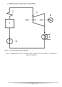
Un sistem se cheamă deschis dacă acesta schimbă cu M.E. şi energie şi
substanţă.
Exemplu de sistem deschis:
Figura 1.2
Boiler în care apa caldă încălzeşte
un curent de apă rece
Un sistem se numeşte adiabatic atunci când schimbul energetic sub
formă de căldură cu alt sistem sau cu M.E., prin suprafaţa sa delimitatoare
este imposibil.
- 6 -
1.2. STARE. PARAMETRII DE STARE. ECHLIBRU
Starea unui S.T. se poate determina prin măsurarea directă a unui
număr (restrâns) de mărimi fizice caracteristice, numite mărimi de stare.
Starea în care valoarea mărimilor de stare nu variază în timp se
numeşte stare de echilibru.
Totalitatea mărimilor fizice măsurabile ale unui sistem care precizează
starea sistemului la un moment dat reprezintă parametrii de stare (ex:
presiune, temperatură, volum, densitate, etc).
Parametrii macroscopici descriu situaţia unui sistem la un moment dat.
Parametrii macroscopici care descriu echilibrul termodinamic se
numesc parametrii termodinamici (P.T.). Aceştia pot fi:
- dependenţi de cantitatea de substanţă şi se cheamă extensivi sau
aditivi (ex: volumul, entalpia, entropia);
- independenţi de masă şi se numesc intensivi (ex: temperatura,
presiunea, etc);
- externi, depind de relaţiile sistemului cu M.E.;
- interni, reprezentaţi de mărimi care depind de proprietăţile interne ale
corpurilor sistemului (ex: presiunea, temperatura, densitatea);
1.3. ECUAŢIA CARACTERISTICĂ (TERMICĂ) DE STARE
Între parametrii termodinamici care caracterizează starea unui sistem,
există o legătură observată experimental de forma:
f ( p,v,T ,...) = 0 (1.1)
Această relaţie permite determinarea unuia dintre parametrii de stare
p, v,T , dacă se cunosc valorile celorlalţi doi parametrii care caracterizează
o anumită stare de echilibru a sistemului.
La sistemele simple, la care variază un singur parametru extern
(volumul), ecuaţia (1.1) devine:
p = p (v,T ) (1.2)
iar sub formă de diferenţială:
T v p
p T v 1
Preview document
Conținut arhivă zip
- Termotehnica.pdf