Extras din laborator
Termenul de “crioscopie” provine din limba greaca si insemna “analiza inghetului”.
Scaderea punctului de inghet reprezinta fenomenul de micsorare, de coborare a punctului de inghet a unui lichid ( solvent ) atunci cand un alt component este adaugat in solutie, acest lucru ducand la un punct mai mic de inghet a solutiei nou formate fata de cel al solventului in stare pura, cum ar fi de exemplu apa. Fenomenul poate fi cu usurinta observat in apa de mare, care datorita sarii pe care o contine reuseste sa ramana in stare lichida chiar si la temperauri mai scazute de 0 grade (temperatura la care apa pura ar ingheta).
Crioscopia este o metoda folosita pentru determinarea masei moleculare a unei substante. Se bazeaza pe determinarea scaderii temperaturi de inghet a unei solutii fata de temperatura de solidificare a solventului pur. Se folosesc pentru aceasta termometre diferentiale (termometrul Beckman), care permit aprecierea unei variatii de temperatura de 0,001 oC. Cunoscand constanta crioscopica (K) a dizolvantului si coborarea temperaturii de solidificare a solutiei ΔT, se poate determina masa moleculara (M) a substantei dizolvate, cu ajutorul relatiei:
ΔT = K * (1000*g1 / M*g2)
(unde g1 este cantitatea de grame de dizolvant, iar g2 cantitatea in grame de substanta dizolvata)
Explicatia
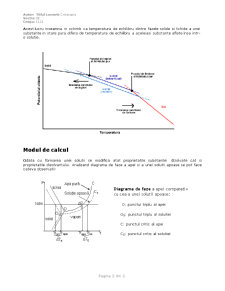
Modificarea potentialului chimic atunci cand o solutie este adaugata intr-un solvent explica cum are loc scaderea punctului de inghetare.
Modificarea punctului de inghet este o proprietate dependenta de prezenta particulelor dizolvate precum si de numarul acestora, nu insa si de natura lor. Este efectul diluarii in solvent a unei cantitati de substanta. Acest fenomen apare la toate substantele, in toate solutiile, chiar si in cele ideale si nu depinde de nicio interactie anume intre solvent si substanta diluata. ( De aceea exlpicatiile conform carora moleculele substantei diluate ar “impiedica” cumva moleculele solventului sa se solidifice nu sunt fondate.)
Modificare punctului de inghet are loc si atunci cand solutia dizolvata este una de electroliti (acizi, baze sau saruri) si atunci cand aceasta nu este una de electroliti. In termeni termodinamici, originea modificarii punctului de inghet este una de natura entropica si este usor de explicat cu ajutorul potentialului chimic al solventului.
La punctul de inghet (sau de topire) starea solida si cea lichida au acelasi potential chimic, ceea ce inseamna ca sunt echivalente din punct de vedere energetic. Potentialul chimic este depedent de temperatura, asa se face ca la alte temperaturi, fie faza solida, fie faza lichida, au un potential chimic mai scazut si sunt deci preferae din punct de vedere energetic celeilalte faze.
In majoritatea cazurilor o substanta se dizolva doar intr-un solvent lichid, nu si intr-unul solid. Asta inseamna ca in cazul unor astfel de substante, potentialul chimic al solventului in faza lichida scade in urma dizolvarii, dar potentialul chimic al aceluiasi solvent in faza solida, nu este afectat.
Acest lucru inseamna in schimb ca temperatura de echilibru dintre fazele solide si lichide a unei substante in stare pura difera de temperatura de echilibru a aceleiasi substante aflate insa intr-o solutie.
Modul de calcul
Odata cu formarea unei solutii se modifica atat proprietatile substantei dizolvate cat si proprietatile dizolvantului. Analizand diagrama de faze a apei si a unei solutii apoase se pot face cateva observatii:
Diagrama de faze a apei comparativ cu cea a unei solutii apoase:
O: punctul triplu al apei
OS: punctul triplu al solutiei
C: punctul critic al apei
CS: punctul critic al solutiei
Presiunea de vapori a solutiilor, Pi, este mai mica cu ΔP decat presiunea de vapori a solventului pur, P0, iar scaderea de presiune este proportionala cu fractia molara a substantei dizolvate, Xi. Acest enunt este cunoscut ca Legea lui Raoult
Preview document
Conținut arhivă zip
- Crioscopia.doc