Extras din laborator
Vp=25mL
c=0.1N=0.05mol/L
Se consideră a≅b
V0=18.6mL
V0 – volum initial de Na2S2O3 (mL)
Vp – volum probă (mL)
Vt – volum de Na2S2O3 la momentul t (mL)
c – concentrația soluției de Na2S2O3 (mol/L)
a – concentrația initial a actonei (mol/L)
b – concentrația inițială a HCl (mol/L)
c’HCl – concentrația HCl înainte de amestecare (mol/L)
V’HCl – volumul HCl înainte de amestecare (mL)
k – consanta de viteză (L/mol•min)
km – constanta medie de viteză (L/mol•min)
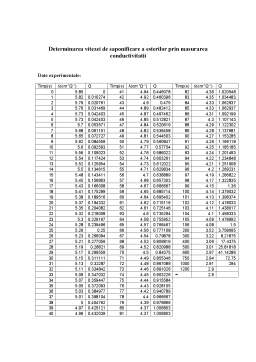
Nr. t (minute) V (mL) x (104•mol/L) k
(104•L/mol•min) km
(104•L/mol•min)
1 0 18.6 0 -
7.0226
2 15 18 1.2 8.3299
3 30 17.5 2.2 7.6357
4 45 17.15 2.9 6.7102
5 60 16.42 4.36 7.5663
6 75 16.3 4.6 6.3863
Concluzii:
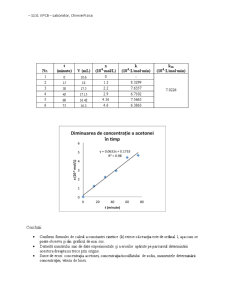
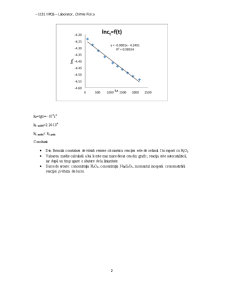
- Conform formulei de calcul a constantei cinetice (k) reiese că reacția este de ordinal I, așa cum se poate observa și din graficul de mai sus.
- Datorită numărului mic de date experimentale și a erorilor apărute pe parcursul determinării acestora dreapta nu trece prin origine.
- Surse de erori: concentrația acetonei, concentrația tiosulfatului de sodiu, momentele determinării concentrației, viteza de lucru.
Preview document
Conținut arhivă zip
- Chimie Fizica
- 1. Cinetica iodurarii acetonei.doc
- 2.Lab apa oxigenata olivia2.doc
- 3.Cinetica enzimatica.doc
- 4.Determinarea spectrofotometrica a vitezei fin.doc
- 5.Determinarea inversiei zaharozei fin.doc
- 56C1A18F.tmp
- Apa oxigenata.xls
- Complex Oxalo Manganic.xls
- Lab CF iodur acetonei.xls
- saponificare.doc