Extras din laborator
Lucrare nr 1
Studiul cinetic al reactiei dintre acidul sulfuric si tiosulfatul de sodiu. Determinarea ordinului partial de reactie si a constantei aparente de viteza de reactie
1.Notiuni teoretice
∑▒〖Vi.Ai〗→∑▒〖〖Vi〗^,〖Ai〗^,〗 , legea vitezei de reactie V=(-1)/(v:) dc1/∆t=1/(v:) 〖dc:1〗^,/∆t (1)
In aceasta lucrare se vor calcula ordinul partial de reactie n_(〖Na〗_2 S_2 O_3 ) si constanta aparenta de viteza de reactie Ka pentru reactie.
Na2 S2 O3+H2 SO4→〖Na〗_2 〖SO〗_4+〖SO〗_2+S+H_2 O
Viteza de reactie in raport cu concentratia sulfurica este data in relatie:
V=(DC_3)/∆t=KC_(H_2 〖SO〗_4)^(n_(〖H_2〗_(〖SO〗_4 ) ) ) C_(〖Na〗_2 S_2 O_3)^(〖n_Na〗_2 s_2 O_2 )=KC_1^(n_1 ) C_2^(n_2 ) (2)
2.Partea experimentala
Se introduc in patru eprubete solutii de tiosulfat de diferite concentratii obtinute confor indicatiilor din tabelul 2.1
Nr
eprubetei Volumul in ml Concentratia sol.
C2=a/(a+b) Volum
H2SO4 ml
Na2S2O3 H2O
1 6 0 1 -
2 4 2 2/3 -
3 3 3 1/2 -
4 2 4 1/3 -
5,6 -
7,8 - - - circa 6ml
Tab. 2.1
In alte patru eprubete se introduce solutie de H2SO4 (circa 6 ml in fiecare eprubeta).
Se vor folosi solutii de Na2S2O3→ 75 g/l si H2SO4 concentrat (ρ=1,83 g/〖cm〗^3) – 15 n1/1.
Timpul de reactie este considerat timpul scurs de la amestecarea reactantilor pina la aparitia primelor particule de precipitat. Dupa pregatirea celor 8 eprubete cu solutie se trece la efectuarea reactiei chimice si la masurarea timpului pina la aparitia primelor particule de precipitat.
Peste continutul eprubetei 1 se toarna solutie de H2SO4 din eprubeta 5, se agita usor si se masoara timpul scurs (∆t) din momentul amestecarii, pina la aparitia opalescentei; se procedeaza similar cu eprubetele 2-6, 3-7, 4-8 si se noteaza valorile ∆t. Se va lua in considerare faptul ca sulful coloidal, care rezulta in urma reactiei devine observabil in momentul cind concentratia acestuia atinge o anumita valoare. Acestei valori ii corespunde in toate experientele variatia ∆c a concentratiei reactantului (Na2S2O3).
Se poate alege, in mod arbitrar, marimea ∆c ca unitate de masura a variatiei concentratiei (∆c=1). In aceste conditii viteza de reactie este numeric egala cu valoarea reciproca a intervalului de timp scurs din momentul amestecarii reactantilor si prina in momentul cind apar particule vizibile de sulf coloidal.
Pentru calculul vitezei de reactie se va utiliza relatia
V=1/∆t
3. Rezultate experimentale
a) Date inregistrare.
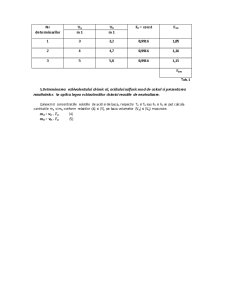
Datele experimentale si cele calculate se inregistreaza in tabelul 2.2
Nr
eprubetei Conc. sol
Ma2S2O3
C2=a/(a+b)
Timp
∆t
(s) Viteza
V=1/∆t
lgv Lgc2
1 1 21
2 2/3 26
3 1/2 39
4 1/2 44
Tab.2.1
4.Prelucrarea datelor experimentale
a) Se traseaza graficul dependentei vitezei reactiei de concentra solutiilor de Na2S2O3 utilizate in cele patru experiente.
b) Se traseaza graficul |-1g∆t|=f(1gc2). Din panta si ordonata la gine a dreptei se calculeaza n2=n_(〖Na〗_2 S_2 O_3 ) si Ka.
c) Caracterizarea statistica a datelor experimentale
Pentru caracterizarea statistica a datelor experimentale se folosesc marimile:
X,S2 si S.
Preview document
Conținut arhivă zip
- Lucrari Laborator Chimie
- Lucrare nr 1.docx
- Lucrare nr 2.docx
- Lucrare nr 3.docx
- Lucrare nr 4.docx
- Lucrare nr 5.docx
- Prima pagina.docx