Extras din laborator
1. Scopul : separarea in fracţii a amesteculuui de heptan - xilen şi determinarea compoziţiei fiecărei fracţii obţinute în prima şi a doua distilare, folosind digrama “Indecele de refracţie - compoziţie”.
2. Principalele noţiuni teoretice:
Prin procedeul distilării simple nu se separă sufficient componentele unui amestec alcătuit din două sau mai multe lichide, chiar dacă diferenţa dintre punctele de fierbere e considerabilă.Pentru aceasta se aplică distilarea fracţionară.
Distilarea fracţionară permite separarea în fracţii a unui amestec de lichide cu diferite puncte de fierbere prin condensarea parţială a vaporilor şi întoarcerea condenstatului cu punctual de fierbere mai înalt în balonul de distilare. Vaporii fracţiei mai volatile vor trece in refrigerent, se vor condensa şi se vor scurge în recipient.
Distilarea se numeşte fracţionară, deoarece amestecul de lichide supus distilării este colectat în diferite recipiente, adică se obţin mai multe fracţii care fierb într-un anumit interval de temperaturi şi nu au punct de fibre constant ca substanţele individuale. Primele fracţii sunt mai bogate cu substanţa ce are punctual de fierbere jos, iar ultimele fracţii conţin substanţa cu cel mai înalt punct de fierbere într-o proporţie mai mare.
Bazele teoriei distilării fracţionare au fost puse de savantul rus D.P.Konovalov, care a descoperit două legi importante.
Principalele raţionamente ale teoriei distilării fracţionare:
Dacă are loc evaporarea unui amestec alcătuit din două sau mai multe componente miscibile în orice proporţii, atunci partea de masă a fiecărei componente în condensatul care se formează este direct proporţională cu partea de masă a acestei componente în amestecul iniţial şi cu presiunea vaporilor ei saturaţi în stare pură.
În cazul evaporării unui amestec binar – din două lichide care au puncte de fierbere diferite, în stare de vapori vor trece ambele componente, însă compoziţia vaporilot se v-a deosebi de compoziţia amestecului de lichide. În faza vaporilor se v-a conţine mai mult componenta cu punctual de fierbere mai jos ( cu presiunea vaporilor mai mare ). Dacă în amestec partea de masă a lichidului cu punctul de fierbere mai jos este mai mare, atunci şi temperature de fierbere a amestecului va fi mai joasă.
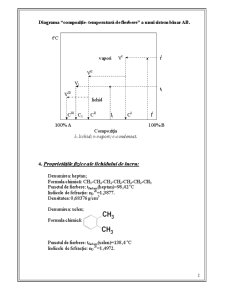
Distilarea fracţionară a unui sistem binar poate fi analizată detailat cu ajuorul diagramei “compoziţie – temperatură de fierbere”. Pe axa ordonatelor se pune temperature de fierbere, iar pe axa abciselor – compoziţia amestecului la presiune constantă. Una dintre curbele diagramei exprimă dependeţa temperaturii de fierbere cu compoziţia amestecului în faza lichidă, iar alta – dependenţa temperaturii de fierbere de compoziţia amestecului în fază de vaporii.
Diagrama “compoziţie- temperatură de fierbere” a unui sistem binar AB.
toC
vapori VI tI
VII
V1
t1
VIII
lichid
CIII C1 CII l1 CI lI
100% A 100% B
Compoziţia
l- lichid; v-vapori; c-condensat.
4. Proprietăţile fizice ale lichidului de lucru:
Denumirea: heptan;
Formula chimică: CH3-CH2-CH2-CH2-CH2-CH2-CH3
Punctul de fierbere: tfierbere(heptan)=98,42 oC
Indicele de fefracţie: nD20=1,3877.
Densitatea: 0,68376 g/cm3
Denumirea: xelen;
Formula chimică:
Punctul de fierbere: tfierbere(xelen)=138,4 oC
Indicele de fefracţie: nD20=1,4972.
Preview document
Conținut arhivă zip
- Distilare Fractionara.doc