Extras din laborator
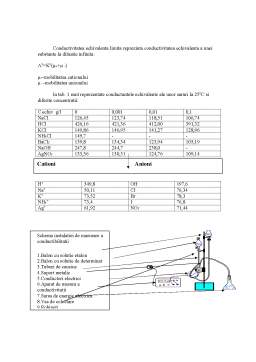
Metoda de analiza conductometrica este utilizata in special pentru determinarea punctului de echivalenta in reactiile de neutralizare si precipitare care sunt insotite de variatii ale concentratiei ionilor cu mobilitati diferite.
Marimea fizica care sta la baza metodei este conductanta:
G= (&)
O solutie de electrolit prezinta o anumita rezistenta electrica atunci cand este strabatut de un current I generat de o diferenta de potential U.aceasta rezistenta poate fi scrisa sub forma :
R= (&)
Á-rezistivitatea (&cm);
l-distanta dintre electrozii cufundati in solutie (cm);
S-sectiunea electrozilor (cm2).
Raportul: K= se numeste constanta celulei.
Conductanta se mai exprima prin relatia:
G= =
Ç-conductivitatea (conductanta specifica)
Ç= [Ç]S.I=¼Scm-1
Ç: -distilate 1¼Scm-1
-demineralizate 0,1….1¼Scm-1
-distilate 5……10¼Scm-1
-potabile 100…..200¼Scm-1
-dure 200…..1500¼Scm-1
Conductivitatea echivalenta › reprezinta raportarea conductivitatii la concentratia solutiei de electrolit:
›= (&-1cm-1 echiv/l)
Preview document
Conținut arhivă zip
- Determinarea Conductivitatii Probelor de Apa.doc