Extras din laborator
Lucrare de laborator nr. 1
A.Studiul procesului de nitrozare după variația concentrației de NO2-
Generalități:
Azotul este unul dintre cele mai importante elemente chimice pentru creșterea și dezvoltarea plantelor. Plantele primesc cantitatea necesară de azot, sub formă de săruri de azot din sol. Deseori pentru stimularea creșterii plantelor agricultorii utilizează îngrășăminte minerale compuse pe bază de azot. În plante el este supus unui proces metabolic complicat. Nitrații reprezintă un produs intermediar în acest proces. Toate plantele conțin o anumită cantitate de nitrați. Deseori ei se gasesc în sursele de ape freatice sau subterane. Pentru sănătatea umană nitrații nu prezintă nici un pericol. În cazul unei diete normale un individ poate ingera zilnic circa 100 mg nitrat și 3 mg nitrit. Pericolul apare în momentul cînd nitrații în organism sub acțiunea fermenților se reduc în nitriți. Nitriții sunt cei care intoxică organismul. Odata ajunși în sînge, nitriții interacționează cu hemoglobina și îi blochează funcția respiratorie, transformînd o parte din ea în methemoglobină, care nu este capabilă să transporte oxigen. În cantități mari, nitrații au efect de iritare a mucoasei gastro-intestinale.
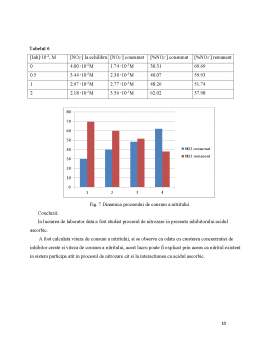
Această proprietate a organismului uman de a reduce nitrații în nitriți depinde de o gamă largă de factori și este strict individuală. Nu a putut fi stabilită o corelație strînsă dintre cantitatea de nitrați primită de om cu produsele alimentare pe parcursul zilei și ponderea methemoglobinei în sînge. Cu toate acestea s-a constatat că la intoxicația cu nitriți sunt expuși unui risc sporit copii pînă la 2 ani. În scopul reducerii hazardului nitriților asupra organismului uman, sau, mai corect spus, a nitriților și a derivaților sai, cantitatea de nitrați în legume și fructe se reglementează în dependență de frecvența și cantitatea medie de produs utilizat în rația alimentară zilnică. În acest context, toate produsele agricole sunt supuse certificării sanitare. Cantitate de nitrați integrată poate fi redusă semnificativ prin organizarea corectă a rației alimentare.
Metoda de analiză a nitriților cu utilizarea reactivului Griess
Reactivi: Reactivul Griess (amestec de acid sulfanilic și α-naftilamină dizolvat în acid acetic glacial) DMA, [NO2-], acid Citric, Na2HPO4.
OBSERVAȚIE: Reactivul Griess se păstrează închis ermetic la întuneric, cel mult o săptămînă.
Pentru analize sistematice ale conținutului de nitriți în apă sunt recomandate metodele spectrofotometrice cu utilizarea reactivului Griess. La fel se utilizează și metoda de diazotare- cuplare cu reactivi modificați.
Această metodă este utilizată pentru determinarea nitriților cu conținutul de la 0,007 pina la 0,35 mg N/l.
Principiul metodei se bazează pe interacţiunea aminelor primare aromatice cu nitriţii în mediul acid cu formarea sărurilor de diazoniu. Drept rezultat al cuplării acestor săruri cu compuşi aromatici, ce conţin grupa OH- sau -NH2, se obţin coloranţii azoici intensiv coloraţi cu nuanţă roz-roşietică.
În metoda elaborată de Griess, se utilizează acidul sulfanilic (4-aminobenzosulfoacid) şi
1-naftilamina. Mecanismul acestui proces are loc după următoarea schemă:
Metoda Griess are o sensibilitate destul de înaltă. Coeficientul de extincţie la max=530 nm alcătuieşte 3,3104. Intensitatea culorii creşte direct proporţional cu [NO-2] în intervalul 10-600g/dm3 calculat pentru NO-2 şi intervalul 3-180 g/dm3 calculat pentru azot. Unul din neajunsurile acestei metode este utilizarea reactivului toxic -naftilamina.
Modul de lucru:
Condiții:
a. Temperatura - 370C;
b. Volumul total - 30 ml;
c. [DMA]- 1*10-2M
d. [NO2-]- 1*10-4M
e. pH-ul – 2,6.
Prepararea soluțiilor:
Tabelul 1
Reactivi Prepararea
Triptofan 1,1021 g de C11H12N2O2 se dizolva intr-un balon 50 ml→[Triptofan]=1∙10-2M
[NO2-] 0,069 g de NaNO2 se dizolvă într-un balon de 100 ml→[NO2-]=1∙10-2g/ml
Ac. Citric 1,921 g de ac. Citric se dizolvă în 100 ml apă distilată
Na2HPO4 7,17 g de Na2HPO4∙12H2O se dizolvă în 100 ml de apă distilată
Reactivul Griess 10 g de reactiv Griess se dizolvă în 100 ml de sol. ac. Acetic de 12%
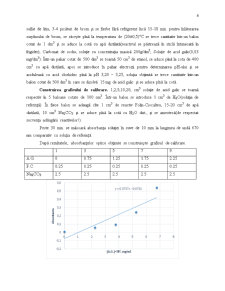
Soluțiile-etalon de nitrit de sodiu; 0,069 g nitrit de sodiu se cîntăresc cu precizie de 0,001 g și se trec cantitativ cu apă înyr-un balon cotat de 100 cm3; după dizolvare completă, se aduce la cotă cu apă distilată și se omogenizează prin agitare; din această soluție se iau cu pipeta 1 cm3, se introduc într-un balon cotat de 100 cm3, se aduce la cotă cu apă distilată și se agită. Soluția-etalon de nitrit se prepară în ziua analizei.
Preview document
Conținut arhivă zip
- Studiul Procesului de Nitrozare dupa Variatia Concentratiei de NO2
- Lucrare de laborator nr 5.docx
- Lucrare de laborator nr. 4 terminata.docx
- Lucrare de laborator nr. 4.docx
- Lucrare de laborator nr.1.docx
- Lucrarea de laborator nr 2.docx
- Lucrarea de laborator nr 3.docx