Cuprins
- 1. Generalităţi 4
- 2. Clasificare 5
- 2.1 Hidruri ale metalelor 5
- 2.2 Hidruri ale nemetalelor si semimetalelor 6
- 3. Metode de preparare 7
- 4. Hidruri 12
- 4.1. Hidruri nemetalice şi semimetalice 12
- 4.1.a Hidruri de tipul HX 12
- 4.1.b Hidruri de tipul H2E 18
- 4.1.c Combinaţiile cu hidrogenul ale elementelor din grupa aVa 26
- 4.1.d Hidrurile de siliciu si germaniu 35
- 4.1.e Hidrurile borului 36
- 4.2 Hidruri metalice 40
- 4.2.a. Hidruri ionice 40
- 4.2.b. Hidruri covalente 42
- 4.2.c. Hidruri interstiţiale 43
- 4.2.d. Hidruri intermediare intre cele ionice sau covalente 45
- 4.2.e. Hidruri anionice 46
- 5. Întrebuinţări 47
- 6. Aplicaţii 48
- 7. Bibliografie 63
Extras din licență
GENERALITĂŢI
Hidrogenul este considerat cel mai răspândit element din univers (93-94%), fiind pus în evidenţă, spectroscopic, în cromosfera soarelui, în stele şi nebuloase.
Pe planeta noastră, hidrogenul se găseşte în cantitate mică în stare liberă în gazele vulcanice, în stratul superior al atmosferei, în gazele naturale şi gazul petrolier.
Intră în componenţa unei mari varietăţi de compuşi din regiunea mineral, vegetal şi animal. Din compuşii cunoscuţi în prezent, marea majoritate conţin hidrogen.
Printre aceştia, apa şi hidrocarburile constituie compuşii cei mai răspândiţi şi mai bogaţi în hidrogen.
Nume, Simbol, Număr atomic Hidrogen, H, 1
Densitate 0.0899 kg/m3
Aspect gaz incolor
Masa atomică 1.00794 u.a.m.
Rază atomică 25 pm
Configuraţie electronică 1s1
Stare de agregare gaz
Punct de topire 14,025 K (−259,125 °C)
Punct de fierbere 20,268 K (−252,882 °C)
Capacitate calorică 14304 J/(kg • K)
Presiune vapori 209 • 103 Pa
Potenţial de ionizare 1312 kJ/mol
Uşor inflamabil
2. CLASIFICAREA HIDRURILOR
După natura elementelor ce se pot combina cu hidrogenul, distingem două categorii de hidruri:
- hidruri ale metalelor ;
- hidruri ale nemetalelor şi semimetalelor ;
2.1. HIDRURI METALICE
Datorită particularităţilor electronice ale atomului de hidrogen care dispune de un singur orbital atomic 1s, neavând nivele electronice interioare şi posedând electronegativitatea 2, 1, comparabilă cu a borului şi carbonului, hidrogenul se combină, în condiţii bine determinate cu majoritatea metalelor, formând hidruri, combinaţiile cele mai simple ale elementelor, cu o mare varietate de tipuri structurale şi proprietăţi specifice. De fapt, hidruri veritabile conţinând ionul hidrură H¯ sunt numai combinaţiile hidrogenului cu metalele puternic electropozitive .
Compuşii hidrogenului cu celelalte metale, în special tranziţionale care nu conţin ionul hidrură sunt sisteme complexe, interstiţiale, formate din mai multe faze, în general nestoechiometrice care uneori capătă proprietăţi analoage aliajelor, numindu-se impropriu hidruri. Limitele între aceste categorii nefiind întotdeauna bine conturate, o clasificare a lor riguroasă este greu de realizat.
Totuşi în linii mari distingem:
- hidruri ionice ;
- hidruri covalente ;
- hidruri interstiţiale ;
- hidruri intermediare între cele interstiţiale şi cele ionice sau covalente ;
- hidruri anionice ;
2.2.HIDRURI NEMETALICE ŞI SEMIMETALICE
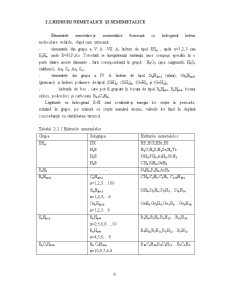
Elementele nemetalice şi semimetalice formează cu hidrogenul hidruri moleculare volatile, după cum urmează:
- elementele din grupa a V A -VII A, hidruri de tipul EHn , unde n=1,2,3 sau E2H4, unde E=N,P,As. Totodată se înregistrează existenţa unor compuşi specifici la o parte dintre aceste elemente , fară corespondenţă în grupă : H2O2 (apa oxigenată), H2S2 (sulfanii), As2 S2, As4 S2 ;
- elementele din grupa a IV A hidruri de tipul SinH2n+2 (silani), GenH2n+2 (germani) şi hidruri polimere de tipul (SiH)n, (SiH2)n, (GeH)n şi (GeH2)n;
- hidrurile de bor , care pot fi grupate în borani de tipul BnHn+4, BnHn+6, borani ciclici, policiclici şi carborani Bn-2C2Hn;
Legăturile cu hidrogenul E-H sunt covalente şi energia lor creşte în perioade, scăzând în grupe, pe măsură ce creşte numărul atomic, valorile lor fiind în deplină concordanţă cu stabilitatea termică .
Preview document
Conținut arhivă zip
- Combinatiile Elementelor cu Hidrogenul.doc