Extras din proiect
Grupa a III a principal cuprinde urmatoarele elemente: bor, aluminiu, galiu, indiu si taliu.Aceste elemente au trei electroni pe stratul exterior: unul din orbitalul np si doi pe orbitalul ns.Primul este un metalloid tipic, iar taliu are character metallic;in ceea ce priveste caracterul chimic al celorlalte trei elemente apar comportari intermediare, dar predomina caracterul metallic.
Borul apare legat covalent in combinatiile sale fiind hibridizat sp2, iar prezenta speciilor chimice cu electroni neparticipanti, avand un orbital vacant nehibridizat, este legat coordinative, schimbandu-si hibridizarea in sp3. Tendinta de cedare a electronilor de valenta este mai mica pentru elementele din aceasta grupa comparative cu a elementelor din grupa I A si II A. Aluminiul si galiul formarea covalente cu halogenii, azotul, carbonul si este electrovalent in compusii sai cu oxigenul, in timp ce taliul fiind practice electropozitiv este legat electrovalent in majoritatea compusilor sai.
Aliuminiul, galiul si indiul au stari de oxidare 1+, 2+ si 3+;in cazul taliului compusii cei mai stabili sunt aceea in care taliul are starea de oxidare 1+. Proprietatea unor elemente de a fosrma compusi stabili, in care valenta elementului este cu doua unitati mai mica decat valenta elementelor din grupa, a fost explicate de Sidgwic prin prezenta perechii de electroni “inerti” din orbitalul s a stratului exterior, caracterizati prin energie mai mica decat a electronului din orbitalul p.
Borul formeaza compusi in care are stare de oxidare 3+. Energia necesara formarii ionului B3+ este mai mare decat aceea care ar putea fi realizata din reactiile chimice la care participa borul si din aceasta cauza nu sunt cunoscuti compusii formati din acesti ioni. Compusii ca BPO4, BaAsO4 nu sunt saruri si oxizi mixti covalenti.
In combinatiile sale borul este hibridizat sp2 si sp3.In compusii lor,celelalte elemente, pe langa hibridizarea sp2 si sp3 apar si in stare de hibridizare sp3d2. Borul, aluminiul si galiul se caracterizeaza prin deficient de electroni in compusii lor covalenti, ei fiind hibridizati sp2, iar un orbital p este vacant:
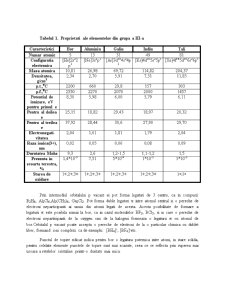
Unele proprietati ale elementelor din grupa III-a principal se gasesc in tabelul 1
Tabelul 1. Proprietati ale elementelor din grupa a III-a
Caracteristici Bor Aluminiu Galiu Indiu Tali
Numar atomic 5 13 31 49 81
Configuratia electronica [He]2s22p1 [Ne]3s2p1 [Ar]3d104s24p1 [Kr]4d105s25p1 [Xe]4f145d106s26p1
Masa atomica 10,81 26,98 69,72 114,82 204,37
Densitatea, g/cm3 2,34 2,70 5,91 7,31 11,85
p.t.,0C 2200 660 29,8 157 303
p.f.,0C 2550 2270 2070 2000 1457
Potential de ionizare, eV pentru primul e 8,30 5,98 6,00 5,79 6,11
Pentru al doilea e 25,15 18,82 29,43 18,97 20,32
Pentru al treilea e 37,92 28,44 30,6 27,90 29,70
Electronegati-vitatea 2,04 1,61 1,81 1,79 2,04
Raza ionica(3+), nm 0,02 0,05 0,06 0,08 0,09
Durutatea Mohs 9,3 2,6 1,2-1,5 1,1-1,2 1,5
Prezenta in scoarta terestra, % 1,4*10-3 7,51 5*10-4 1*10-5 1*10-5
Starea de oxidare 1+;2+;3+ 1+;2+;3+ 1+;2+;3+ 1+;2+;3+ 1+;2+
Prin intermediul orbitalului p vacant ei pot forma legaturi de 3 centre, ca in compusii: B2H6, Al2Cl6,Al2(CH3)6, Ga2Cl2. Pot forma duble legaturi π intre atomul central si o pereche de electroni neparticipanti ai unuia din atomii legati de acesta. Acesta posibilitate de formare a legaturii π este posibila numai la bor, ca in cazul moleculelor BF3, BCl3, si in care o pereche de electroni neparticipanti de la oxygen sau de la halogeni formeaza o legatura π cu atomul de bor.Orbitalul p vacant poate accepta o pereche de electroni de la o particular chimica cu dublet liber, formand ioni complexi ca de exemplu: [BH4]-, [BF4]-etc.
Preview document
Conținut arhivă zip
- Tehnici de Analiza Chimica cu Aplicatii in Industria Alimentara.docx