Cuprins
- 1.Prezentarea generală a acetonei 4
- 2.Structura grupării carbonil 5
- 3. Metode de obținere 5
- 3.1.Dehidrogenarea alcoolului izopropilic 5
- 3.2.Oxidarea alcoolului izopropilic la acetona. 6
- 3.3. Dehidrogenarea directă 7
- 3.4.Variabilele de proces la dehidrogenarea alcoolului izopropilic 8
- 3.5.Catalizatori folosiți în procesul de dehidrogenare a alcoolului izopropilic 9
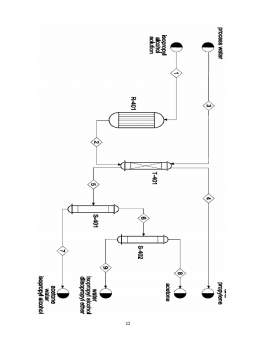
- 3.6. Schema tehnologică simplificată de obținere a acetonei prin dehidrogenarea alcoolului izopropilic 10
- 3.7 Medota cumenică 11
- 4. Proprietăți fizico-chimice 13
- 4.1. Proprietăți fizice 13
- 4.2. Proprietăți chimice 14
- 4.2.1. Adiția apei 14
- 4.2.2. Aditia alcoolilor 15
- 4.2.3. Adiția hidrogenului 15
- 4.2.4. Adiția hidracizilor 16
- 4.2.5. Adiția acidului cianhidric 16
- 4.2.6. Aditia compusilor organometalici, urmata de hidroliza conduce la alcooli 16
- 4.2.7.Reactia de condensare a acetonei 16
- 4.2.8. Oxidarea acetonei 18
- 4.2.9.Reacția Meerwein-Ponndorf-Verley (1925) 18
- 5.Pericolele reactivului chimic 19
- 5.1.Pericole pentru om/sănătate 19
- 5.2 Pericole pentru mediu 20
- 5.3. Măsuri de prim ajutor 21
- 6.Măsuri de combatere a incendiilor 22
- 7.Măsuri de luat în caz de dispersie accidentală 22
- 8. Manipulare și depozitare 23
- 9.Informații referitoare la transport 23
- 10.Informatii toxicologice si ecologice 24
- 10.1 Informații toxicologice 24
- 10.2 Informatii ecologice 25
- 11.Scopul utilizarii acetonei 27
- RAPORT DE EXPERTIZĂ 28
- 1.Preambul 28
- 2.Sursa litigiului 28
- 3.Istoricul litigiului 28
- 4. Obicetivele expertizei 30
- 5.Procedura de investigație 30
- 6.Studierea documentelor operative 31
- 7. Constatările expertizei 31
- 8.Concluzii 32
- ANEXE 33
Extras din proiect
Acetona (dimetil cetona sau propanona), este un compus organic cu formula CH3-CO-CH3. Acesta este un lichid incolor cu miros caracteristic,fiind utilizat ca solvent organic pentru acetatul de celuloza, nitroceluloza și acetilena, dar și ca reactant într-o serie de procese de termoliza și reacții de sinteză în chimia organică. Face parte din grupa cetonelor. Caracteristic pentru strucutura acetonei este gruparea carbonilică de care se leagă două grupări metil.
Acetona se găsește în cantități mici în sângele uman și ăn urină. La diabetici continutul de acetone în urină este mai mare datorită descompunerii acidului acetoacetic.
Prima dată a fost obținută în anul 1755 de Libavius prin distilarea uscată a acetatului de plumb. Natura și structura ei corecta a fost determinată în 1832 de către Liebig și Dumas.
Cererea tot mai mare de acetonă a condus la dezvoltarea altor procedee bazate pe surse petroliere și ăn special propilena. Începând din anul 1920, acetona s-a obținut în special prin dehidrogenarea alcoolului izopropilic. Dupa 1953, o dată cu apariția procedeului de obținere a fenolului prin oxidarea cumenului, acetona s-a obținut ca co-produs alături de fenol. În 1961 s-a dezvoltat un nou procedeu de obținere a acetonei din propilenă.
Lichid incolor cu miros dulceag în concentrații mai ridicate, înțepător, ușor inflamabil, în combinație cu aerul formează un amestec exploziv. Se dizolva în orice proporții cu apa și majoritatea solvenților.
2.Structura grupării carbonil
Atomul de carbon al grupării carbonil este hibridizat sp2, la fel ca atomii de carbon ai legăturii olefinice, unghiurile C-C-C și C-C-O la acetonă fiind apreciate la valoarea de 120o. Legătura σ C-O se formează prin întrepătrunderea unui orbital hibrid sp2 al atomului de carbon cu orbitalul 2px al atomului de oxigen. La rândul ei legătura π se formează prin întrepătrunderea laterală a orbitalului nehibridizat 2pz al oxigenului cu orbitalul 2pz al carbonului.
Legătura dublă C=O este o legătură puternică, cu o energie de 179 kcal, mai mare chiar decât dublul energiei legăturii simple C-O ( 2x85,5 kcal). În comparație cu legătura C=C, care posedă o energie de 145,8 kcal, hidrogenarea dublei legături C=O are loc mai încet și este mai puțin exotermă.
Grupa carbonil este un cromofor, adică o grupare de atomi , cu caracter nesaturat, care introdusă în molecula unei substanțe organice incolore o transformă într-o substanța colorată.
3. Metode de obținere
3.1.Dehidrogenarea alcoolului izopropilic
Acest procedeu reprezintă cea mai importantă sursă de obținere a acetonei și este folosit și în prezent. Există mai multe variante ale acestui procedeu și anume:
- dehidrogenarea directă a alcoolului isopropilic sau
- oxidarea acestuia cu aer conform reacțiilor:
CH3-CHOH-CH3 → CH3-CO-CH3 + H2 -16kcal/mol
CH3-CHOH-CH3 + 1/2O2 → CH3-CO-CH3 + H2O +42kcal/mol
Diferența dintre aceste două reacții constă în faptul că, în primul caz se obține ca produs secundar hidrogenul, iar în a doua reacție apa.
3.2.Oxidarea alcoolului izopropilic la acetona este o cale mai putin folosită, întrucat se obțin randamente mai scăzute, iar pe de altă parte hidrogenul obținut în procesul de dehidrogenare a alcoolului izopropilic este un produs valoros, care contribuie la reducerea costurilor de fabricație ale acetonei. Reacția de oxidare are loc într-un reactor ca cel de la dehidrogenare și se face la temperaturi mai ridicate 500-600șC , consumul de combustibil este asemănător, întrucat reacția este exotermă. Drept catalizator se utilizează cupru metalic sau argint. Faza lichidă constituită din acetona brută este supusă purificarii prin distilare.
Oxidarea alcoolului izopropilic la acetona poate decurge și pe altă cale,prin hidroxihidroperoxid de propan.
Reacția are loc la temperatura de 95-140 șC și presiune de 3 atm, într-un reactor tip coloană, în care alcoolul izopropilic proaspăt și recirculat se introduc pe sus, iar oxigenul este alimentat pe la partea inferioară. Reacția este exotermă, preluarea căldurii de reacție făcându-se prin refluxarea acetonei și alcoolului izopropilic.
Din alcoolul izopropilic, acetona se mai poate obține printr-o reacție de transhidrogenare, care convertește acroleina la alcool alilic:
Preview document
Conținut arhivă zip
- Raport de expertizare - Acetona.doc