Cuprins
- CAPITOLUL I – Noţiuni introductive .2
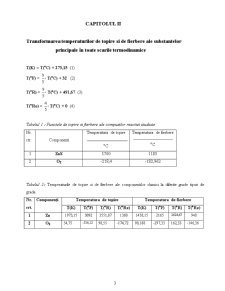
- CAPITOLUL II – Transformarea temperaturilor de topire şi de fierbere ale substanţelor principale în toate scările termodinamice .4
- CAPITOLUL III – Entalpia de reacţie .5
- a. Calculul entalpiei de reacţie în condiţii standard.5
- b. Aprecieri asupra stabilităţii compusului obţinut în comparaţie cu alţi compuşi similari .6
- c. Determinarea dependenţei entalpieie de reacţie în funcţie de temperatură .7
- d. Particularizarea şi trasarea grafică a dependenţei entalpiei la temperaturile de 330K, 530K, 730K şi 930K pentru 1 mol substanţă principală respectiv 200 kg substanţă principală .8
- CAPITOLUL IV – Entropia de reacţie .12
- a. Calculul entropiei de reacţie în condiţii standard .12
- b. Aprecieri calitative asupra entropiei de reacţie .13
- c. Determinarea dependenţei entropiei de reacţie în funcţie de temperatură .13
- d. Particularizarea şi trasarea grafică a dependenţei entropiei la temperaturile de 330K, 530K, 730K şi 930K pentru 1 mol substanţă principală respectiv 200 kg substanţă principală .13
- CAPITOLUL V – Energia liberă Gibbs .17
- a. Calculul energiei libere Gibbs în condiţii standard .17
- b. Aprecieri asupra spontaneităţii procesului în sistem izolat/neizolat .17
- c. Determinarea dependenţei energiei libere Gibbs în funcţie de temperatură .18
- d. Particularizarea şi trasarea grafică a dependenţei energiei libere Gibbs la temperaturile de 330K, 530K, 730K şi 930K pentru 1 mol substanţă principală respectiv 200 kg substanţă principală .18
- CAPITOLUL VI – Afinitatea de reacţie .21
- CAPITOLUL VIII – Concluzii privind deplasarea ecuaţiei chimice .22
- CAPITOLUL IX – Bibliografie .23
Extras din proiect
CAPITOLUL I
Notiuni introductive
Termodinamica studiaza din punct de vedere energetic proprietatile generale ale substantelor si legile care guverneaza miscarea termica fara a tine seama de natura miscarilor şi interactiilor moleculare.
Chimia fizica este o ramura importanta a chimiei alaturi de Chimia organica, Chimia anorganica, Chimia macromoleculara, Chimia analitica.
Reactia asupra careia se va efectua studiul termodinamic este urmatoarea:
ZnS + 2O2 ↔ ZnSO4
Sulfura de zinc
Zincul sulfurat ( sulfura de zinc) este un compus chimic cu formula ZnS. Zincul sulfurat are culoarea alb-galbena . Este, de obicei intalnit in forma mai stabila cilindrica, cunoscut ca zinc blende sau sphalerite, de asemenea este intalnit si sub forma hexagonala.Este cunoscut atat in calitate de material sintetic si in calitate de minerale wurtzite.
ZnS a fost utilizat de catre oamenii de stiinta in primii ani de fizica nucleara ca un detector de stralucire, pentru ca acesta emite lumina pe excitatie de raze X sau fascicul de electroni, ceea ce il face util pentru ecrane si tuburi cu raze catodice. De asemenea, prezinta o fosforescenta datorita impuritati pe iluminare cu lumina albastra sau ultravioleta.
Figura 1:Reprezinta
sulfura de zinc
Oxigenul la standard de temperatura şi presiune este un gaz incolor, inodor cu formula moleculara O2. Oxigenul este mai solubil in apa decat azotul apa contine aproximativ o molecula de O2 pentru fiecare 2 moleculele de N2, comparativ cu un raport atmosferic de aproximativ 1:4. Solubilitatea oxigenului in apa este dependenta de temperatura. Fotosinteza pleaca de la apa si CO2 pentru a degaja O2 .Organismele vii folosesc 70% din oxigenul produs gratuit de pe pamant, iar restul este produs de plantele terestre, O2 este esential pentru respiratie(intretine viata pe pamant). Un adult inhaleaza 1.8 la 2.4 grame de oxigen pe minut. Aceasta se ridica la mai mult de 6 miliarde de tone de oxigen inhalat de umanitate pe an
Sulfatul de zinc (ZnSO4) este un cristalin incolor, solubil in apa.Este intalnit si sub forma hidratata, ZnSO4* 7 H2O. Istoric, a fost cunoscut sub numele de "alb vitriol" si poate fi pregatit prin adaugare de zinc peste acid sulfuric apos. De asemenea, poate fi preparat prin adaugarea de zinc solid la o solutie de sulfat de cupru II. (Zn + CuSO4 → ZnSO4 + Cu). Acesta este utilizat pentru a furniza zinc in ingrasaminte agricole si spray-uri. ZnSO4 *7 H2O este utilizat in calitate de conservant pentru piei si piele si in medicina ca astringent şi vomitiv.
Figura 2:Reprezinta sulfatul de zinc
Preview document
Conținut arhivă zip
- Studiul Termodinamic al Reactiei Sulfurii de Zinc cu Oxigenul.doc