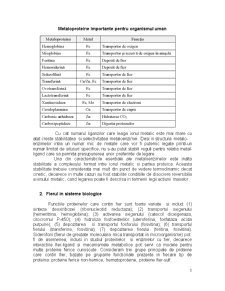
Extras din proiect
Enzimele, compusi biologici macromoleculari, cu proprietati catalitice, produse exclusiv de celulele vii, sunt holoproteine cu structuri tridimensionale specifice, alcatuite numai din lanturi polipeptidice, de aminoacizi sau heteroproteide, care contin, pe linga componenta proteica, termolabila, nedializabila, cu proprietati fizico-chimice specifice proteinelor, denumita apoenzima si o componenta neproteica, termostabila, cu masa moleculara mica si dializabila, denumita cofactor enzimatic.
Activitatea catalitica a enzimelor este limitata la o regiune mica a componentei proteice, numita centru activ sau situs catalitic activ. Numeroase enzime contin in situsul lor activ ioni metalici sau necesita prezenta ionilor metalici pentru trecerea enzimei din starea de zimogen, inactiva, in stare catalitic activa.
Enzimele in care ionii metalici sunt puternic incorporati si legati stoechiometric in structura lor, fara a putea fi eliminati in procesul de purificare al enzimei, se numesc metaloenzime.
Metaloproteinele, compusii ai cationilor metalici cu moleculele organice
de interes biologic, sunt heteroproteine in care componenta prostetica este
reprezentata de un metal, iar componenta proteidica este constituita dintr-o catena in care exista gruparile polare libere apartinand poliheteroaminoacizilor
constituenti. Structura chimica specifica macromoleculelor de metaloproteine
confera acestora proprietati functionale in care specificitatea are importanta aparte. Gruparile polare din catenele macromoleculare concura la stabilirea legaturilor cu metalele din componenta prostetica. Acest considerent explica relatia structura chimica in activitate biologica, precum si prezenta numeroaselor metaloproteine ca bioconstituenti celulari si tisulari sau ca efectori in reactiile biochimice specifice proceselor metabolice. Metalele care au fost puse in evidenta frecvent in structura metaloproteinelor sunt: fier, cupru, mangan, zinc, cobalt, magneziu etc. Legatura dintre metal si apoproteina se realizeaza prin intermediul gruparilor polare libere ale aminoacizilor din molecula proteica.
Se considera ca apoproteina prezinta o anumita regiune din molecula
susceptibila de a stabili legaturi cu metalul, in conformitate cu distributia spatiala a gruparilor capabile sa formeze asemenea legaturi. Metalul (M2+) se fixeaza de
apotroteina prin liganzi, grupari care pot dona electroni metalului, stabilindu-se
astfel legaturi covalente coordinative, metalul devenind coordinat. Prin intermediul liganzilor, metalul fixat pe apoproteina formeaza un complex intern numit chelat care se caracterizeaza prin existenta unui ciclu in care se stabilesc covalente coordinative intre atomii de N sau O ai ligandului si ionul metalic coordinat. Existenta acestor structuri cu caracter de chelat sunt posibile in metaloenzime, structuri care explica mecanismul functional al acestora in procesele biochimice la care intervin.
Preview document
Conținut arhivă zip
- Importanta Fierului in Sisteme Biologice.doc