Cuprins
- CUPRINS 2
- I . ENUNTAREA CELUI DE AL DOILEA PRINCIPIU AL TERMODINAMICII 3
- II.TRANSFORMĂRI CICLICE 4
- III. CICLUL CARNOT 6
- IV. INTEGRALA LUI CLAUSIUS PENTRU CICLU ŞI EVOLUŢIE REVERSIBILE 7
- Pentru ciclu reversibil 7
- Pentru o evoluţie reversibilă 8
- Concluzii: 9
- V. INTEGRALA LUI CLAUSIUS PENTRU CICLU ŞI EVOLUŢIE IREVERSIBILE 9
- Pentru ciclu ireversibil 9
- Pentru evoluţie ireversibilă 10
- Concluzii: 10
- VI. Semnificaţia entropiei şi expresia matematică a PT2 11
- 6.1 Frecarea, cauză a ireversibilităţii proceselor 12
- 6.2 Calculul variaţiei de entropie 12
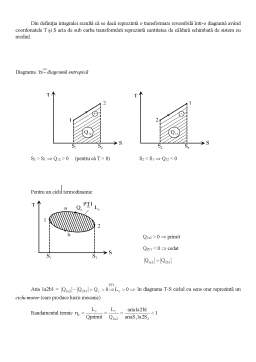
- 6.3 Diagrame entropice 14
- Reprezentarea transformărilor în diagrama T-s 15
- Transformarea adiabată 15
- Transformarea izotermă 16
- Transformarea izocoră (v = const, dv = 0) 16
- Transformarea izobară 17
- Transformarea politropă 17
- Reprezentarea grafică a mărimilor calorice de stare 18
- 6.4 Exergie si Anergie 18
- Randamentul exergetic 19
- Bibliografie 21
Extras din proiect
I . ENUNTAREA CELUI DE AL DOILEA PRINCIPIU AL TERMODINAMICII
Primul principiu al termodinamicii afirmă că în cazul în care un sistem izolat efectuează o evoluţie, energia sistemului se conservă. În particular, în cazul sistemului care schimbă căldură şi lucru mecanic cu mediul exterior în timpul unui ciclu (U = 0) există o echivalenţă între căldură şi lucru mecanic schimbat cu exteriorul.
Dar P T l nu precizează ce cantitate de căldură disponibilă poate fi transformată în lucru mecanic într-un ciclu dat, după cum nu poate preciza sensul de desfăşurare al unei evoluţii în anumite condiţii date.
Se constată experimental însă că în natură fenomenele au un anumit sens de desfăşurare de la sine, spre exemplu difuzia se realizează din zona cu concentraţie mai mare spre zona cu concentraţie mai mica, transferul de căldură de la corpul cu temperatură mai ridicată spre cel cu temperatură mai mică, curgerea gazelor de la o presiune mai mare spre presiune mai mică etc. Aceste transformări se numesc naturale. O transformare poate fi realizată în sensul invers celui natural cu consum exterior de energie, adică dacă apar modificări permanente în exterior.
Toate aceste constatări experimentale reflectă de fapt principiul al doilea al termodinamicii care are ca obiective :
1) să stabilească ce parametri caracterizează o evoluţie naturală;
2) dacă dintr-o cantitate de căldură dată putem sau nu să transformăm în lucru mecanic, prin intermediul unui ciclu, întreaga cantitate de căldură a disponibilă.
Cele mai cunoscute formulări ale P T 2, care de fapt sunt echivalente între ele, sunt următoarelec
a) Căldura nu poate trece de la sine de la corpul cu temperatură mai mică la cel cu temperatură mai mare.
b) O maşină termică nu poate produce în mod continuu, adică ciclic, lucrul mecanic decât dacă agentul de lucru schimbă căldură cu două surse de căldură de temperaturi diferite.
Maşina care ar transforma continuu în lucru mecanic căldura luată de la o singură sursă de căldură fără să cedeze o parte altei surse reci se numeşte perpetuum mobile de speţa a II-a.
c) Un perpetuum mobile de speţa a II-a este imposibil.
II.TRANSFORMĂRI CICLICE
În cadrul studiului transformărilor simple s-a constatat că la destinderea unui gaz, se poate obţine lucru mecanic, iar la comprimarea gazului se consumă lucrul mecanic. Dacă se doreşte să se producă lucru mecanic în mod periodic, este necesar ca gazul să fie readus, după destinderea sa, din nou in starea iniţială, după care se poate relua procesul. Readucerea în stare iniţială nu se poate însă efectua pe acelaşi drum pe care s-a realizat destinderea, deoarece în acest caz întregul lucrul mecanic produs ar fi din nou consumat. O astfel de transformare se numeşte transformare ciclică sau ciclu termodinamic. În urma parcurgerii unui ciclu, toate mărimile de stare ale sistemului revin la valoarea iniţială.
În diagrama p-V din figura 4.1, curba adiabatei (q = 0) împarte diagrama în două zone. Transformările care pornesc de pe curba adiabatei spre stînga si cele care pornesc spre dreapta vor avea pentru căldura schimbată semne diferite.
Figura 4.1
În diagrama p-V un ciclu termodinamic se reprezintă printr-o curbă închisă.
Exemplu: izocora 1-3 (dv = 0) q = du + pdv = du = cvdT q = cvdT
Ecuaţia izocorei 1-3 p3 > p1 T3 >T1 T3 - T1 > 0 T > 0 dT > 0
Dacă dT > 0, din q = cvdT q > 0
Deci pentru transformările care pleacă de pe curba adiabatei spre dreapta q > 0 iar pentru cele care pleacă spre stânga q < 0.
Indiferent de curba ciclului, se pot trasa 2 adiabate tangente la curba închisă a ciclului.
Dacă se parcurge ciclul în sensul 1a2b1, pe porţiunea 1 a 2 sistemul primeşte căldura Q1 din exterior iar pe porţiunea 2 b 1 sistemul cedează căldura Q2 în exterior.
De asemenea, lucrul mecanic pe evoluţia 1 a 2 este aria de sub curba 1 a 2 iar pe evoluţia 2 b 1, aria de sub curba 2 b 1. Deci lucrul mecanic efectuat de sistem pe parcursul întregului ciclu va fi diferenţa ariilor, adică aria suprafeţei mărginită de curba închisă a ciclului (Lc).
Din expresiile matematice ale PTl (2.5, 2.6): Q = dU + L = dI + Lt
Integrând după conturul închis:
,
(pentru că U şi I sunt mărimi de stare, deci revin la valoarea iniţială)
Adică, pentru o transformare ciclică, lucrul mecanic al ciclului = suma căldurilor schimbate = suma lucrurilor mecanice exterioare = suma lucrurilor mecanice tehnice.
Deci în cazul transformării ciclice dispare diferenţa între lucrul mecanic exterior şi cel tehnic.
Dacă ciclul este parcurs în sens orar L1 a 2 > L2 b 1 Lc > 0 deci se produce lucru mecanic ciclul se numeste motor. Dacă ciclul este parcurs în sens trigonometric, Lc 0, ciclul se numeste ciclu generator, fiind un ciclu consumator de lucru mecanic.
Preview document
Conținut arhivă zip
- Principiul al Doilea al Termodinamicii.doc