Cuprins
- Cuprins
- Capitolul I. Memoriu tehnic 2
- Capitolul II. Tehnologia de fabricație 3
- II.1. Domeniile de utilizare și proprietățile produsului 3
- II.2. Variantele tehnologice 14
- II.3. Alegerea variantei optime 18
- II.4. Descrierea procesului tehnologic adoptat 19
- Materii prime, intermediare și auxiliare 28
- Mecanismul reacțiilor biochimice 33
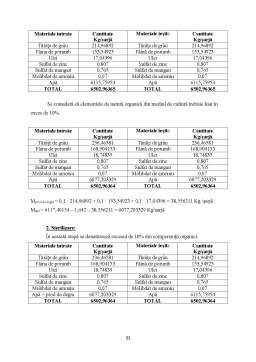
- Bilanţul de materiale 51
- Capitolul III Controlul fabricației 58
- III.1. Controlul, reglarea și automatizarea procesului tehnologic 58
- III.2. Controlul de calitate 62
- Capitolul IV Produse secundare, deşeuri de fabricaţie, epurarea apelor reziduale 70
- Capitolul V Transport, ambalare, depozitare 72
- Capitolul VI Utilităţi 73
- Capitolul VII Norme de protecţia muncii, de prevenirea şi stingerea incendiilor 75
- Bibliografie 79
Extras din proiect
Capitolul I. Memoriu tehnic
Industria biochimică se caracterizează printr-un ritm rapid de dezvoltare, în ultimele decenii luând o amploare deosebită. Se observă pe plan mondial o creştere a cerinţei de produse obţinute prin biosinteză: proteine, vitamine, medicamente, enzime,
Lucrarea de faţă prezintă un studiu asupra posibilităţii de obţinere a proteazelor de natură bacteriană.
În capitolul II, tehnologia de fabricaţiei, s-a făcut o prezentare a produsului, s-au tratat câteva probleme legate de enzime în general şi de enzime proteolitce în particular, s-au prezentat variantele de obţinere a proteazelor din care s-a ales varianta optimă.
În continuare, s-a realizat descriere procesului tehnologic adoptat, s-a descris cinetica şi termodinamica procesului şi sa realizat bilanţul de materiale pe intreg procesul tehnologic.
În următorul capitol, III, sunt evidenţiate aspecte legate de automatizarea instalaţiei şi de control al materiilor prime, intermediare şi al produsului finit.
În capitolul IV, s-au cuprins câteva probleme referitoare la valorificarea produselor secundare, asupra deşeurilor de fabricaţie şi epurarea apelor reziduale.
Capitolul V, s-a axat pe partea de transport , ambalare şi depozitare a produselor secundare si final.
Următorul capitol, VI, din cadrul acestui proiect face referire şi la câteva aspecte referitoare la utilităţi (aburul, apa, aerul, energia electrică).
În ultimul capitol, VII, sunt prezentate câteva Norme de protecţie a muncii şi stingerea incendiilor.
Capitolul II. Tehnologia de fabricație
II.1. Domeniile de utilizare și proprietățile produsului
Enzimologia este o știință care s-a dezvoltat uimitor în ultima perioadă de timp, începuturile ei situîndu-se în primele decenii ale secolului al XIX-lea. Dacă în 1920 erau cunoscute aproximativ 10-15 enzime, prin observarea efectului acțiunii lor, astăzi sunt caracterizate parțial peste 2000 de enzime.
Noțiunea de enzimă începe să se contureze de-abia în 1833 când Payen și Persoz, reluând și dezvoltând observațiile anterioare ale lui Kirchhoff demonstrează prezența unui principiu activ în extractele de orz germinat, care realizează hidroliza amidonului și pe care-l purifică prin precipitări repetate cu alcool etilic pâna la obținerea unei pulbere albe.
În perioada 1834-1837 chimistul suedez Berzelius formulează conceptul de cataliză, conform căruia un catalizator mărește viteza reacțiilor chimice și rezultă la sfârșitul lor, nemodificat cantitativ si calitativ.
În 1877, Kuhn propune numele de enzimă, de la grecescul enzyme, care înseamnă ,,în drojdii’’, pentru toate substanțele descoperite, cu acțiune de catalizator al unei reacții biochimice. Acestă denumire, în acea perioadă la mare concurență cu termenii ,,diastază’’ și ,,ferment’’ este astăzi unanim acceptată și utilizată de biochimiști.
În anul 1926, Sumner cristalizează ureaza extrasă din fasole, demonstrând faptul că enzimele sunt proteine.[1]
O enzimă poate fi definită ca o polipeptidă care catalizează o reacție cu un anumit grad de specificitate. În această definiție se folosesc 3 cuvinte cheie: polipeptidă, cataliză și specificitate.
1. Enzimele ca polipeptide:
Astăzi este acceptat faptul că majoritatea enzimelor sunt proteine. Funcționalitatea enzimelor este o consecință directă a secvențării aminoacizilor în catena polipeptidică (structura primară), a plierii catenei în conformații α-helix, straturi β-pliate sau aperiodic (structură secundară), a interacțiunilor catenelor laterale ale aminoacizilor prin forțe electrostatice, hidrofobe și punți disulfurice (structură terțiară) și al asamblării subunităților proteice (structură cuaternală).
Cu toate că lanțurile polipeptidice ale enzimelor conțin sute de resturi de aminoacizi, doar câteva resturi sunt implicate direct în legarea substratului sau în reacția catalitică. Mai mult, natura reacției care este catalizată de o enzimă dată este dependentă de identitatea aminoacizilor care alcătuiesc centrul activ. Resturile de aminoacizi implicate în formarea centrului activ determină, prin polaritatea și potențialul lor de ionizare, specificitatea și mecanismul de reacție, care sunt caracteristice unei enzime particulare.
În plus, structura, forma și topografia polipeptidei pliate pot asista procesul de ,,captare’’ a substratelor la suprafața enzimei și pot facilita difuzia substratului spre locul de transfomare chimică. Flexibilitatea structurii polipeptidice și interacțiunile cu (micro)mediul înconjurător sunt de asemenea responsabile pentru controlul și reglarea activității enzimei.
2. Proprietățile catalitice ale enzimelor:
Transformarea materiei prin reacții chimice reprezintă unul dintre fenomenele esențiale ale universului. Însăși viața, fie ca este vorba de regnul vegetal, sau animal, depinde de o serie de reacții chimice aflate într-o perfectă corelare. Ridicarea nivelului de trai al omului are la bază aplicațiile industriale ale reacțiilor chimice prin care se obțin energie, alimente, medicamente, fibre textile etc. Însă, de cele mai multe ori aceste reacții chimice decurg totuși prea lent pentru a susține viața sau de a deveni interesante pentru industrie. Pentru aceasta, natura, iar mai târziu omul, au inventat catalizatorii care au rolul de a accelera viteza acestor reacții.
La nivel molecular, orice reacție chimică presupune desfacerea unor legături și formarea altora noi, ceea ce înseamnă că pe parcursul conversie reactanților la produse are loc o variație de energie între starea inițială și cea finală a sistemului.
Preview document
Conținut arhivă zip
- Tehnologia de Obtinere a Proteazelor cu Utilizare in Panificatie.docx