Cuprins
- Capitolul I: Infarctul miocardic acut
- I.1 Fiziopatologie: rolul ruperii acute a placii
- I.2 Prezentare clinica
- I.3 Farmacoterapia infarctului miocardic
- I.4 Aprecierea si controlul riscului postinfarct
- I.5 Preventia secundara a infarctului
- Capitolul II: De la boli coronariene la insuficienta cardiaca: beneficii potentiale ale ivabradinei
- II.1 Legatura dintre frecventa cardiaca si rata mortalitatii si morbiditatii cardiovasculare la pacientii cu boala coronariana
- II.2 Ritmul cardiac si progresia aterosclerozei: o tinta pentru ivabradina
- II.3 Inhibitia curentului If cu ivabradina in cursul spitalizarii dupa infarctul miocardic
- II.4 Ivabradina postdescarcare, dupa infarctul miocardic
- II.5 Inhibitia curentului If cu ivabradina la pacientii cu insuficienta cardiaca
- II.6 Concluzii
- Capitolul III: Ivabradina: primul inhibitor selectiv al canalului nodului sinusal If in tratamentul anginei permanente
- III.1 Notiuni introductive: boala cardiovaculara
- III.2 Rolul curentului If
- III.3 Scaderea ritmului cardiac in angina
- III.4 Optiuni terapeutice in tratamentul cu curenti
- III.5 Curentul If ca tinta farmacologica
- III.6 Experimente realizate pe animale cu ivabradina
- III.7 Studii clinice privind rolul ivabradinei in prevenirea si evolutia anginei
- III.8 Monoterapia cu ivabradina
- III.9 Combinatii terapeutice cu ivabradina
- III.10 Studii despre tolerabilitate
- III.11 Concluzii
- Capitolul IV: Studiul BEAUTIFUL
- IV.1 Explicatia rationala a studiului BEAUTIFUL
- IV.2 Rezultatele studiului BEAUTIFUL
- Capitolul V: Diminuarea cronica a frecventei cardiace: prevenirea disfunctiei endoteliale la soarecii cu dislipidemie
- V.1 Metode
- V.2 Telemetrie
- V.3 Protocoale experimentale
- V.4 Analiza statistica
- V.5 Rezultate
- V.6 Discutii
- Capitolul VI: Reducerea pura a frecventei cardiace: perspective viitoare in insuficienta cardiaca
- VI.1 Explicatia ratinala a reducerii ritmului cardiac la pacientii cu insuficienta cardiaca
- VI.2 Beneficiile scaderii frecventei cardiace in insuficienta cardiaca
- VI.3 Perspective viitoare in insuficienta cardiaca: rolul ivabradinei in scaderea frecventei cardiace
- VI.4 Concluzii
- Capitolul VII: Caz clinic
- VII.1: Optimizarea farmacoterapiei anginei pectorale: maximizarea rezervei cronotrope
- Capitolul VIII: Modul de actiune al ivabradinei
- VIII.1 Electrofiziologie cardiaca: elemente fundamentale esentiale
- VIII.2 Inhibitia selectiva a curentului If cu ivabradina
- VIII.3 Reducerea exclusiva a frecventei cardiace cu ivabradina
- VIII.4 Profil farmacocinetic si farmacodinamic
- VIII.5 Date preclinice de siguranta
- VIII.6 Date clinice
- VIII.7 Farmacologia ivabradinei
- VIII.8 Concluzii
Extras din proiect
Capitolul I
Infarctul miocardic
Infarctul miocardic este unul din cele mai frecvente diagnostice la pacienţii spitalizaţi în ţările industrializate, se produc în fiecare an aproximativ 1,5 milioane de infarcte miocardice. Rata mortalităţii prin infarct acut este de aproximativ 30%, mai mult de jumătate din decese producându-se înainte ca individul afectat să ajungă la spital. Deşi rata mortalităţii după spitalizare pentru infarct miocardic a scăzut cu aproximativ 30 de procente de-a lungul ultimelor două decade, aproximativ l din fiecare 25 de pacienţi care supravieţuiesc la spitalizarea iniţială moare în primul an după infarctul miocardic. Supravieţuirea este marcat redusă la pacienţii vârstnici (peste vârsta de 65 de ani), a căror rată de mortalitate este de 20% la l lună şi de 35% la l an după infarct.
I.1. Fiziopatologie: rolul rupturii acute a plăcii
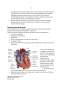
Infarctul miocardic se produce în general când există o scădere bruscă a fluxului sanguin coronarian ca urmare a unei ocluzii trombotice a unei artere coronare stenozată anterior prin ateroscleroză. Stenozele de grad înalt ale arterei coronare, care se dezvoltă lent, nu precipită de obicei infarctul miocardic acut datorită dezvoltării unei bogate reţele colaterale de-a lungul timpului, în schimb, infarctul se instalează când un trombus al arterei coronare se dezvoltă rapid la nivelul sediului unei injurii vasculare. Această injurie este produsă sau facilitată de factori cum ar fi fumatul, hipertensiunea şi depunerea de lipide, în majoritatea cazurilor, infarctul se produce atunci când o placă aterosclerotică se fisurează, se rupe sau se ulcerează, şi atunci când condiţiile (locale sau sistemice) favorizează trombogeneza, astfel încât un tromb mural se formează la nivelul sediului rupturii şi conduce la ocluzia arterei coronare. Studiile histologice indică faptul că plăcile coronare predispuse la ruptură sunt acelea cu miezul bogat în lipide şi cu capsula fibroasă subţire. După ce se formează un monostrat plachetar la nivelul sediului plăcii rupte, o varietate de agonisii (colagen, ADP, epinefrină, serotonină) promovează activarea plachetară. Datorită stimulării agoniste are loc producţia şi eliberarea de tromboxan A2 (un compus capabil să inducă vasoconstricţia), activarea plachetară suplimentară şi rezistenţa potenţială la tromboliză.
În plus faţă de generarea de tromboxan A2, activarea plachetelor de către agonisii iniţiază modificări conformaţionale la nivelul receptorului glicoproteic Hb/IIIa. Odată ce este convertit la starea sa funcţională, acest receptor dezvoltă o afinitate înaltă pentru secvenţa arginină-glicină-acid aspartic (numită secvenţa RGD) de pe lanţul alfa al fibrinogenului, precum şi pentru secvenţa dodecapeptid de pe lanţul gamma al fibrinogenului. Deoarece fibrinogenul este o moleculă multivalenlă, el se poate lega simultan la două plachete diferite, având ca rezultat legătura încrucişată plachetară şi agregarea.
Cascada coagulării esle activală prin expunerea factorului tisular din celulele endoteliale lezate de la nivelul plăcii rupte. Factorii VII şi X suiţi activaţi, conducând în final la conversia protrombinei în trombină, care apoi transformă fibrinogenul în fibrină. Trombina în faza fluidă şi cea limitată de cheag participă la o reacţie de autoamplificare, conducând la activarea în continuare a cascadei coagulării. Artera coronară lezală devine în final ocluzionată printr-un trombus ce conţine agregate plachetare şi depozite de fibrină.
În cazuri rare, infarctul se poate datora ocluziei arterei coronare determinată de embolii coronariene, anomalii congenitale, spasm coronarian şi de o mare varietate de boli sistemice - în special inflamatorii, în cele din urmă, gradul lezării miocardice cauzată de ocluzia coronariană depinde de teritoriul irigat de vasul afectat, de faptul că vasul devine sau nu total ocluzionat, de factorii nativi care pot produce liza spontană precoce a trombusului ocluziv, de cantitatea de sânge asigurat de vasele colaterale către ţesutul afectat şi de cerinţa de oxigen a miocardului a cărui irigaţie sanguină a fost brusc limitată. Pacienţii cu risc crescut de a dezvolta infarct miocardic acut sunt aceia cu angină instabilă sau angină variantă Prinzmetal şi aceia cu multipli factori de risc coronarian. Condiţiile medicale subiacente mai puţin frecvente care predispun pacienţii la infarct includ hipercoagulabilitatea, bolile vasculare de colagen, abuzul de cocaină şi trombii intracardiaci sau tumorile ce pot produce embolie coronariană.
I.3. Prezentare clinica
În aproximativ jumătate din cazuri un factor precipitant pare a fi prezent anterior infarctului miocardic, cum ar fi efortul fizic susţinut, stresul emoţional şi boli medicale sau chirurgicale. Infarctul miocardic poate debuta în orice moment al zilei sau nopţii, dar frecvenţa este mai mare dimineaţa, în primele ore după trezire. Acest vârf circadian se poate datora combinaţiei tonusului crescut simpatic şi tendinţei accentuate la tromboză între orele 6:00 A.M. şi 12 ziua. Durerea este cea mai obişnuită acuză de prezentare a pacienţilor cu infarct miocardic, în unele cazuri, disconfortul poate fi destul de sever pentru a fi descris ca fiind cea mai intensă durere pe care pacientul a simţit-o vreodată. Durerea din infarctul miocardic este profundă şi viscerală; adjectivele utilizate în mod obişnuit pentru a o descrie sunt: greutate, constricţie şi zdrobire, deşi uneori este descrisă ca un junghi sau ca o arsură. Ea are caracter similar cu disconfortul din angină pectorală, dar este de obicei mai severă şi durează mai mult. Tipic durerea se localizează în regiunea centrală a toracelui şi/sau epigastru şi ocazional iradiază către braţe. Localizările mai puţin obişnuite ale iradierii sunt: abdomenul, spatele, mandibula şi gâtul. Localizarea frecventă a durerii mai jos de xifoid şi refuzul pacienţilor de a accepta că ei pot suferi un atac de cord sunt în primul rând responsabile de diagnosticul eronat de indigestie. Durerea din infarctul miocardic poate iradia superior până la regiunea occipitală, dar nu iradiază inferior de ombilic. Este adesea însoţită de slăbiciune, transpiraţie, greaţă, vărsături, anxietate şi senzaţie de moarte iminentă. Disconfortul poate debuta când pacientul este în repaus. Atunci când durerea începe în timpul unui efort, ea nu se atenuează de obicei la încetarea activităţii spre deosebire de angină pectorală.
Deşi durerea este cea mai obişnuită acuză la prezentare, ea nu este neapărat întotdeauna prezentă. Incidenţa infarctelor nedureroase este mai mare la pacienţii cu diabet zaharat şi ea creşte cu vârsta. La vârstnici, infarctul miocardic se poate prezenta ca dispnee apărută brusc, care poate evolua spre edem pulmonar. Alte modalităţi de prezentare mai puţin obişnuite, cu sau fără durere, includ pierderea bruscă a conştientei, stare confuzională, senzaţie de slăbiciune profundă, apariţia unei aritmii, semne de embolie periferică sau numai o scădere inexplicabilă a tensiunii arteriale. Durerea din infarctul miocardic poate simula durerea din pericardita acută, embolia pulmonară, disecţia acută de aortă şi costocondrita. Aceste afecţiuni ar trebui astfel luate în considerare în diagnosticul diferenţial.
Preview document
Conținut arhivă zip
- Diminuarea Cronica a Frecventei Cardiace
- BIBLIOGRAFIE.doc
- cuprins partea generala.doc
- grafice.doc
- Lucrare Finala.doc