Cuprins
- 1. Generalități: 3
- 2. Formele coroziunii zincului 4
- 2.1. Coroziunea galvanică 4
- 2.2. Coroziunea în pitting 5
- 2.3. Coroziunea intergranulară 5
- 2.4. Coroziunea sub forma “petelor de umezeală” 6
- 3. Cauzele coroziunii 6
- 4. Pasivitatea metalelor 7
- 5. Coroziunea zincului în diferite medii 7
- 5.1. Coroziunea zincului în atmosferă 7
- 5.1.1. Influența factorilor atmosferici 10
- 5.2. Coroziunea zincului în apă 12
- 5.2.1. Coroziunea zincului în apa distilată 13
- 5.2.2. Coroziunea zincului în ape menajere 15
- 5.2.3. Coroziunea zincului în apa naturală și de mare 16
- 5.3. Coroziunea zincului în soluri 16
- 5.4. Coroziunea zincului in medii chimice 17
- 5.4.1. Coroziunea în săruri dizolvate, acide și baze 18
- 5.4.2. Coroziunea în medii neapoase 18
- 6. Metode de protecţie 21
- 7. Concluzii 24
- 8. Bibliografie 25
Extras din referat
1. Generalități:
În antichitate, zincul a fost utilizat pentru prima data la obținerea alamei. Producția de alamă a început în vremea Imperiului Roman. Ca metal nou, zincul a fost produs pentru prima dată în India, în secolul al XIII-lea, iar în Europa în anul 1546. Consumul de zinc a crescut încet în secolul al XIX-lea și a ajuns la 0,5 Mt în anii 1900. În secolul XX, consumul de zinc a crescut rapid datorită performanței sale excelente împotriva coroziunii și a naturii nedăunătoare mediului înconjurător. Astfel, în 2002, consumul mondial de zinc a ajuns la 8,926 Mt. [1]
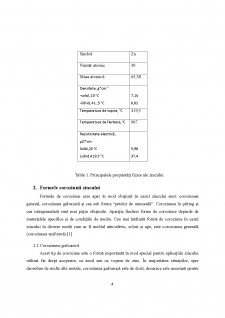
Denumirea de zinc provine din cuvântul german zink. Zincul este un element chimic care are simbolul Zn si numarul atomic 30. Zincul are un aspect gri-albastru în urma expunerii în atmosferă. O foaie de zinc nouă se prezintă cu un aspect asemănător aluminiului. Se obține din minereuri și din compuși, fiind folosit în aliaje cu alte metale pentru protejarea acestora împotriva oxidării (ruginii). Rezistența și duritatea zincului sunt mai mari decât ale plumbului și staniului, dar mai mici decât ale aliminiului și cuprului. Forma sa cristalină este hexagonală HCP ( hexagonal close packed). Principalele proprietăți fizice ale zincului sunt listate în tabelul 1. [3]
Fig.1. Structura hexagonală a zincului [5] Fig.2. Zincul [4]
Simbol Zn
Număr atomic 30
Masa atomică 65,38
Densitate, g*cm-3
-solid, 20 0C
-lichid, 41.,5 0C
7,14
6,62
Temperatura de topire, 0C 419,5
Temperature de fierbere, 0C 907
Rezistivitate electrică, µΩ*cm
Solid,20 0C
Lichid,419.5 0C
5,96
37,4
Table 1. Principalele proprietăți fizice ale zincului
2. Formele coroziunii zincului
Formele de coroziune care apar în mod obișnuit în cazul zincului sunt: coroziunea general, coroziunea galvanică și cea sub forma “petelor de umezeală”. Coroziunea în pitting și cea intergranulară sunt mai puțin obișnuite. Apariția fiecărei forme de coroziune depinde de materialele specifice și de condițiile de mediu. Cea mai întâlnită formă de coroziune în cazul zincului în diverse medii cum ar fi mediul atmosferic, soluri și ape, este coroziunea generală (coroziunea uniformă).[1]
2.1. Coroziunea galvanică
Acest tip de coroziune este o formă importantă în mod special pentru aplicațiile zincului utilizat fie drept acoperire, ca anod sau ca vopsea de zinc. În majoritatea situațiilor, spre deosebire de multe alte metale, coroziunea galvanică este de dorit, deoarece este necesară pentru metalul din pilă, protejat galvanic- care este de obicei oțel. În funcție de metalul cu care este conectat și tipul mediului atmosferic, coroziunea galvanică poate fi de 5 ori mai puternică decât coroziunea normală a zincului în atmosferă rurală și de 3 ori față de cea din atmosfera maritimă.
Bibliografie
1. Coroziunea și protecția anticorozivă a zincului în diferite medii, Alina Prună, Universitatea Politehnica București, 2008
2. Coroziunea și controlul coroziunii, Teodora Badea, Anca Cojocaru, Gabriela Ciura, editura MATRIX ROM, București, 2000
3. https://ro.wikipedia.org/wiki/Zinc
4. https://eucbeniki.sio.si/kemija8/937/index3.html
5. http://minerva.mlib.cnr.it/mod/book/view.php?id=269&chapterid=106
Preview document
Conținut arhivă zip
- Coroziunea zincului in diferite medii.docx