Extras din referat
Au existat in decursul timpului mai multe tentative ale chimistilor de clasificare a elementelor chimice: in metale si nemetale, acizi si baze, in functie de valenta sau de alte proprietati. Aplicarea acestor metode facea insa ca o serie de elemente sa se regaseasca in mai multe grupe concomitent. O clasificare mai detaliata si mai utila s-a bazat la inceput pe greutatea atomica si apoi pe numarul atomic. Aceasta clasificare a condus la ceea ce cunoastem astazi sub denumirea de sistemul periodic, inclus in tabelul periodic care ilustreaza grafic legaturile dintre diferite elemente.
Clasificarea initiala a elementelor cunoscute in metale si nemetale a condus mai departe la diferentieri in functie de reactivitate. S-a observat ca unele elemente au proprietati intermediare intre metale si nemetale, acestea primind denumirea de metaloizi.
Încă din antichitate, aproximativ prin anii 400 î.e.n, în Grecia antică s-au folosit cuvintele "element" şi "atom" pentru a desemna diferenţele dintre diferitele părţi ale materiei şi pentru a desemna părţile cele mai mici care alcătuiesc materia.
În secolul al XVIII-lea, marele chimist francez Antoine Lavoiser, în lucrarea sa "'Traité Elémentaire de Chimie" (Tratat de chimie elementară), apărută în 1789, a împărţit cele 33 de elemente cunoscute la vremea sa în patru grupe în funcţie de proprietăţile lor chimice: gaze, nemetale, metale, şi pământuri
In 1828, J.W. Döbereiner a remarcat ca la unele elemente exista aceeasi diferenta intre greutatea lor atomica (termenul actual utilizat este masa atomica relativa) atunci cind sunt aranjate in grupe de cite trei. De exemplu, a observat aceeasi diferenta intre greutatea atomica a elementelor clor – brom si brom – iod. Pe aceeasi baza a gasit si alte grupari asemanatoare care au devenit cunoscute sub denumirea de “triadele lui Döbereiner”. Cercetătorul francez De Chancourtois a realizat un tabel cilindric al elementelor pentru a arăta reapariţia periodică a proprietăţilor elementelor chimice.
John Newlands a aratat in 1864 ca aceste clasificari sunt parte integranta dintr-o schema mai generala. Newlands a grupat elementele pe linie in ordinea masei lor atomice si atunci cind a observat aparitia unor elemente cu proprietati similare la intervale regulate, a regrupat elementele si in in coloane:
H Li Be B C N O
F Na Mg Al Si P S
Cl K Ca Cr Ti Mn Fe
Newlands a observat ca proprietatile primelor sapte elemente reapar si la urmatoarele sapte, astfel incit primul si al optulea, al doilea si al noulea si asa mai departe, apartin aceluiasi grup sau familii. El a numit acest fenomen “legea octavelor”. Gazele nobile care nu fusesera descoperite pina in anul 1890, si-au gasit locul in aceasta schema la sfirsitul fiecarei linii. Aceasta teorie nu a fost luata in serios la acea vreme mai mult datorita alegerii termenului muzical de “octava” de catre Newlands.
Alte contribuţii la clasificarea elementelor chimice, au mai adus cercetătorul englez Wiliam Olding, în 1864 şi cercetătorul german Julius Lothar Meyer în 1868.
W. Olding a realizat un tabel foarte asemănător cu cel realizat mai târziu de Mendeleev. Grupele sunt aranjate pe orizontală iar elementele sunt aşezate în ordinea masei atomice. În tabel s-au lăsat spaţii libere pentru elementele nedescoperite.
Chimistul german Julius Lothar Meyer a realizat un tabel al elementelor chimice în 1864, apoi o a doua versiune în 1868, elementele fiind aşezate în ordinea masei atomice. Mayer şi-a publicat lucrarea mult mai târziu decât Mendeleev, astfel încât nu a putut avea prioritate în acest domeniu. Se pare că cei doi chimişti, Meyer şi Mendeleev au descoperit sistemul periodic al elementelor în acelaşi timp.
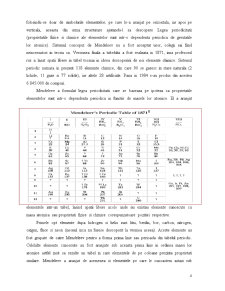
Cel care este unanim acceptat ca fiind descoperitorul sistemului periodic modern al elementelor a fost chimistul rus, Dimitri Ivanovici Mendeleev. In 1869, acesta a prezentat in premiera, in cadrul unei conferinte a Societatii Ruse de Chimie, tabelul periodic al elementelor. Mendeleev a realizat prima varianta a sistemului periodic al elementelor chimice in 17 februarie 1869. Atunci el a ordonat pentru prima data cele 63 de elemente chimice cunoscute la acea vreme in ordinea cresterii maselor atomice. A realizat tabelul folosindu-se doar de simbolurile elementelor, pe care le-a aranjat pe orizontala, iar apoi pe verticala, aceasta din urma structurare ajutandu-l sa descopere Legea periodicitatii (proprietatile fizice si chimice ale elementelor sunt intr-o dependenta periodica de greutatile lor atomice). Sistemul conceput de Mendeleev nu a fost acceptat usor, colegii sai fiind neincrezatori in teoria sa. Versiunea finala a tabelului a fost realizata in 1871, insa profesorul rus a lasat spatii libere in tabel tocmai in ideea descoperirii de noi elemente chimice. Sistemul periodic numara in prezent 118 elemente chimice, din care 90 se gasesc in stare naturala (2 lichide, 11 gaze si 77 solide), iar altele 28 artificiale. Pana in 1984 s-au produs din acestea 6.845.000 de compusi.
Preview document
Conținut arhivă zip
- Evolutia Tabelului Periodic al Elementelor Chimice.doc