Extras din referat
Introducere
Acest articol evalueaza sinergismul dintre bacteriile reducatoare de Fe (IRB), Shewanella putrefaciens si bacteriile sulfat reducatoare (SRB), Desulfovibrio alaskensis.
S-a aratat recent ca GR2(SO42-) a fost present in produsul de coroziune al pilelor de otel, imersate timp de 25 de ani in apa de mare si a fost asociat cu SRB.
Daca formarea GR2(SO42-) este o consecinta a chimiei fierului fata de apa de mare, atunci prezenta sa a contribuit la existenta unei activitati microbiene. Este firesc ca GR2(SO42-) sa se formeze pe cale biotica si poate servi ulterior drept rezervor de sulfat pentru activarea SRB.
Prin urmare tinta acestui articol este de a clarifica trasaturile principale ale mecanismului de biocoroziune. GR2(SO42-) a fost format prin reducerea lepidocrocitului cu S. putrefaciens in atmosfera de hidrohen – ca unica sursa de electroni. Experimentele de alterare a GR2(SO42-) prin D. alaskensis au fost controlate cu GR2(SO42-) biogenic, ca singurul aceptor de electroni si lactatul ca electron – donor, intr-un mediu netamponat. Monitorizarea in functie de timp a produsilor este observata prin transformarea biotica a GR2(SO42-) sub observarea XRD (Difractie de Raze X), TMS (Spectroscopie Mossbauer) si TEM (Spectroscopie de Emisie Electronica).
Metode experimentale
Experimente de reducere a Fe au fost controlate cu S. Putrefaciens si descrise de [2]. GR2(SO42-) rezultat, a fost folosit ca acceptor al electronului in metabolismul SRB. D alaskensis a fost incubat intr-un mediu mineral cunoscut, continand K2HPO4 (0.5 g/L). Lactatul de Na serveste drept sursa de electroni (3.5 g/L). Pentru a caracteriza produsii sunt utilizate trei metode de investigare : DRX, TMS, TEM. Spectrele Mössbauer au fost masurate prin interpretarea constantei de accelerare - 50 mCi de la o sursa de 57Co.
Pe calculator se vor realiza fitarile cu ajutorul programului « Recolil Software « de la Lagarec si Rancourt, utilizand modelul Lorentzian sau pseudo – metoda Voigt, bazata pe metoda celor mai mici patrate. Datele XDR au fost colectate cu un difractometru D8 Bruker, cu monocromator si detector de pozitie. Sursa de raze x a fost un anod de Co (λ=0.17902 nm). TEM s-a realizat folosind CM 20/STEM Philips cu un voltaj de 200 kV.
Rezultate si discutii
Bioreducerea lepidocrocitelor
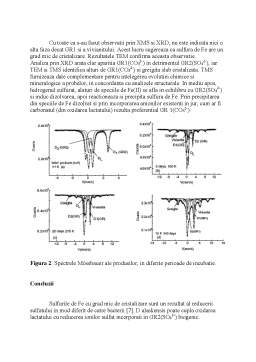
Produsul, colorat in verde, format din γ – FeOOH, prin bioreducere, a fost caracterizat prin XRB si TMS. Inregistrarile care s-au obtinut in urma difractiei de raze X, pentru produsii obtinuti dupa 90 zile de incubatie, arata prezenta GR2(SO42-) si a lepidocrocitelor (Figura 1a).
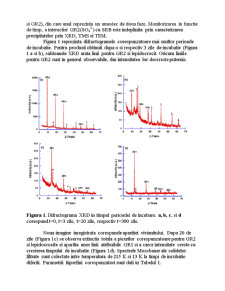
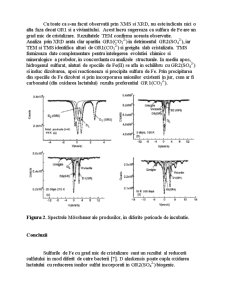
Intervalul experimental (zile) pentru GR2 este similar celui obtinut in conditii biotice si abiotice pentru GR2(SO42-) [2]. Spectrul Mossbauer al fazei de culoare verde, inregistrat la 77 K, poate fi fitat rezonabil (Tabelul 1) cu trei dublete cuadrupol – paramagnetice: D1, D2 si DLepidocrocite (Figura 2a). Dubletele D1 (starea feroasa) si D2 (stare ferica), corespunzatoare GR2 (57 %) si DL sunt atribuite Fe3+ paramagnetic in Lepidocrocite (43 %), cu o mica modificare a izomerului δ (0.47 mm/s) si despicatura cuadrupol cu valoarea ∆ (0.62 mm/s) LA 77 K [2].
Reactivitatea GR2 cu SRB
Pentru GR exista doua tipuri de modele XRD, depinzand de forma anionilor intercalate, care induc secvente variate. GR1 incorporeaza anioni planari sau sferici (Cl-, CO32-), pentru ca in timp ca GR2 insereaza anioni tridimensionali (SO42-), [4]. Compusii GR1 au o structura trigonala cu secventa
Preview document
Conținut arhivă zip
- Monitorizarea Transformarii Structurale a Hidroxi - Sulfatului in Prezenta Bacteriilor Sulfat - Reducatoare.doc