Extras din referat
CAPITOLUL I
PROTEINELE
STRUCTURA SI PROPRIETATI CHIMICE
Proteinele sunt compusi organici naturali cu structura complexa si masa moleculara mare, care, prin hidroliza, se transforma în ±-aminoacizi. Acesti compusi organici naturali sunt considerati ca fiind suportul material al tuturor fenomenelor vietii. De fapt, acestia sunt principalii constituienti cu structura macromoleculara ai protoplasmei tuturor celulelor vegetale si animale. Numarul proteinelor existente în natura este extrem de mare.
Denumirea mentionata deriva de la cuvântul grecesc proteios = fundamental, care sugereaza importanta deosebita a acestor compusi. Proteinele, separate si obtinute în stare pura din produsele naturale, pot fi hidrolizate pe cale chimica sau enzimatica cu obtinerea asa-numitelor hidrolizate proteice în care s-au identificat 20 ±-aminoacizi.
De aceea, în primul rând este important sa cunoastem structura si proprietatile aminoacizilor, componentele de baza ale proteinelor naturale în vederea întelegerii depline a însusirilor si functiilor fiziologice ale proteinelor
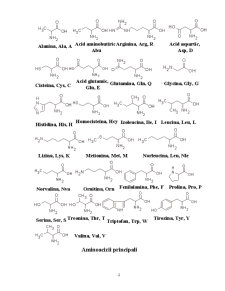
I.1. Aminoacizii, componente esentiale ale proteinelor
Proteinele contin un numar de 20 de a-aminoacizi, numiti si aminoacizi standard. Cu exceptia prolinei, acestia au o grupare amino si una carboxil legate de atomul de carbon a. Aminoacizii se deosebesc între ei prin structura catenelor lor laterale, numite radicali R.
Exista patru clase de aminoacizi: 1) aminoacizi cu radicali nepolari sau hidrofobi; 2) aminoacizi cu radicali polari neutri (grupari neîncarcate); 3) aminoacizi cu radicali încarcati pozitiv si 4) aminoacizi cu radicali încarcati negativ (la pH fiziologic normal de 6,0 - 7,0). În cadrul fiecarei clase, exista variatii mari în ceea ce priveste marimea, forma si proprietatile radicalilor R.
a) Aminoacizi hidrofobi sunt alanina, leucina, izoleucina, valina si prolina dintre cei alifatici, fenilalanina si triptofanul dintre aromatici si un aminoacid cu sulf, metionina. Componentul cel mai hidrofob este alanina, iar prolina difera de ceilalti aminoacizi prin structura sa, fiind un a-iminoacid.
b) Aminoacizii cu radicali polari neîncarcati sunt relativ solubili în apa si contin grupari polare neutre ce pot genera legaturi de hidrogen. Acestia sunt serina, treonina si tirozina, ce contin gruparea hidroxil si asparagina si glutamina ce contin gruparea amidica capabila de a forma legaturile de hidrogen. De asemenea, cisteina formeaza legaturi polare prin gruparea sulfhidril, SH. La limita se gaseste glicina sau glicocolul, care are un R = H care nu poate influenta hidrofobicitatea moleculei.
c) Aminoacizii cu radicali încarcati pozitiv (bazici)
La pH 7 acesti aminoacizi prezinta sarcini pozitive, nete. Între acestia sunt lizina, cu gruparea e-NH2, arginina care prezinta o grupare guanidinica încarcata pozitiv, histidina, care contine gruparea imidazol slab bazica. Histidina, de fapt, este singurul aminoacid al carui radical R are pK' aproapiat de 7,0.
I.1.1. Proprietatile aminoacizilor
Aminoacizii au puncte de topire sau de descompunere ridicate, de regula peste 200ºC. Acestia sunt mai solubili în apa decât în solventi nepolari. Reteaua moleculara a aminoacidului în stare cristalina este stabilizata prin forte electrostatice de atractie între grupari cu sarcini opuse ca în cazul retelelor cristaline ale sarurilor cu puncte de topire ridicate. Asadar, aminoacizii se gasesc în solutii apoase neutre si cristalizeaza din aceste solutii ca ioni dipolari sau amfioni si nu ca molecule nedisociate. Existenta aminoacizilor sub forma de ioni dipolari în solutii apoase neutre este indicata si de constantele dielectrice înalte si momentele de dipol mari, care arata prezenta sarcinilor electrice diferite în aceeasi molecula. Astfel de substante sunt amfotere si sunt numite amfoliti, forma prescurtata de la electroliti amfoteri.
Preview document
Conținut arhivă zip
- Lucrare Stiintifica.doc