Cuprins
- 1. Introducere 3
- 2. Proprietăți fizice și chimice 3
- 3.Toxicitate și efect asupra mediului 5
- 4. Utilizări 6
- 4.1. Solvent 6
- 4.2. Monomeri acrilici 6
- 4.3. Bisfenol A 7
- 4.4. Produse chimice aldolice 7
- 4.5. Alte utilizări 8
- 5. Metode de obținere 8
- 5.1. Oxidarea cumenului ( Procesul Hock ) 9
- 5.2. Dehidrogenarea 2-propanolului 13
- 5.3. Oxidarea propenei 14
- 5.4. Oxidarea 2-propanolului 15
- 5.5. Oxidarea p-diizopropil benzenului 15
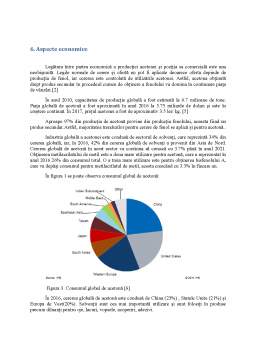
- 6. Aspecte economice 16
- Bilbliografie 18
Extras din referat
1. Introducere
Acetona, denumită și 2-propanona sau dimetilcetona este primul și cel mai important membru din seria omoloagă a cetonelor alifatice. Aceasta eate incoloră, lichidă și utilizată pe scară largă drept solvent pentru o varietate de polimeri. Cea mai importantă utilizare a ei însă este drept intermediar în sinteza metacrilatului de metil, a bisfenolului A , etc.
Acetona a fost prima dată sintetizată prin distilarea uscată a acetatului de calciu. Acetatul de calciu era obținut prin distilarea lemnului, iar mai târziu a fost obținut prin fermentația etanolului. În anul 1920, aceste procese au fost înlocuite de distilarea directă a carbohidraților la acetonă, alcool butilic și etilic. Apoi, în anii 1950-1960 au fost înlocuite și aceste procese de dehidrogenarea 2-propanolului și oxidarea cumenului la fenol și acetonă. Împreună cu oxidarea directă a propenei, aceste metode acoperă 95% din producția de acetonă la nivel mondial.[1]
În plus, aceasta este un solvent doarte bun pentru o mare varietate de rășini, ceruri, grăsimi, uleiuri, vopsele, materiale celulozice. Este folosită pentru transportul acetilenei, în producția a numeroase materiale plastice și acoperiri și drept materie primă pentru sinteza unei varietăți de produse chimice: cetena, metil-metacrilat, bisfenol A, alcool diacetonic, izobutil cetona, hexilenglicol și izoforona.
Producția acetonei în 1990 era estimată la 3 milioane de tone metrice pe an, din care 1 milion în Statele Unite. Existând numeroase surse naturale de acetonă, aceasta este un constituent normal în mediul înconjurător și este ușor biodegradabilă.[2]
2. Proprietăți fizice și chimice
Acetona este un lichid incolor, foarte inflamabil și infinit solubil în apă. Vaporii de acetonă au un miros caracteristic floral și dulce la concentrații mici.[3] Principalele proprietăți fizice și termodinamice sunt prezentate în tabelele 1 și 2:
Tabel 1. Proprietăți fizice ale acetonei[2]
Nr.crt Proprietăți fizice/chimice
1 Masa moleculară 59.08
1 Temperatura de îngheț -94.6°C
2 Temperatura de fierbere 56.29 °C
3 Indice de refracție la 20°C 1.3588
4 Solubilitatea în apă 100% la 20°C
5 Conductivitatea electrică 5.5*10--8 S/cm
6 Volum critic 0.209 L/mol
7 Presiunea critică 4701 kPa
8 Temperatura critică 235.05 °C
9 Densitate 0.784 kg/m3
10 Vâscozitate 0.4 cP
Tabel 2. Proprietăți termodinamice ale acetonei[2]
Nr.crt Proprietăți termodinamice
1 Căldura specifică a lichidului la 20°C 2.6 J/g
2 Căldura specifică a vaporilor la 102°C 92.1J/(mol*K)
3 Căldura de vaporizare la 56.1°C 29.1 kJ.mol
4 E ntalpia de vaporizare 30.836 kJ/mol
5 Entropia lichidului 200.1 J/(mol*K)
6 Entropia gazului ideal 295.349 J/(mol*K)
7 Energia Gibbs de formare -152.716 kJ/mol
În ceea ce privește proprietățile chimice, acetona reacționează conform reacțiilor tipice ale cetonelor saturate alifatice. Aceasta formează compuși cristalini precum bisulfitul de sodiu al acetonei cu bisulfiții alcalini. Prin reducerea acetonei se poate obține alcool izopropilic sau propan. Prin amonoliză reductivă se pot obține amine izopropilice.Acetona este stabilă în prezența multor agenți oxidanți precum soluția Fehling, azotat de argint, acid azotic rece sau permanganat de potasiu, dar poate fi oxidată cu alți oxidanți mai puternici precum permanganat alcalin, acid cromic, acid azotic cald. În prezența unor halogeni, se pot obține halocetone. Compușii cu un hidrogen activ sunt adiționați la gruparea carbonil a acetonei, apoi urmând de obicei condensarea cu o alta moleculă și eliminarea apei.
Aceasta este un produs metabolic în organismul uman și în unele organisme animale, fiind un constituent normal în sânge și urină. În plus, acesta se formează în exces în organismele bolnave de diabet.
.[2]
Acetona are limitele de inflamabiliate între 2.13% și 13%, iar temperatura de autoaprindere este 465°C. Inflamabilitatea acesteia poate fi redusă prin amestecarea cu solvenți mai puțin inflamabili sau volatili. În condiții puternic bazice, acetona reacționează cu acidul cianhidric, formând 2-ciano 2-propanol, un intermediar important în sinteza esterilor metacrilici, de exemplu metacrilatul de metil. În soluție de amoniac , acetona condensează cu acetilena în prezența unor metale alcaline și formează 2-metil-3-butin-2-ol, acesta fiind un intermediar important în sinteza izoprenului.
Alte reacții importante sunt hidrogenarea catalitică a acetonei pentru obținerea 2-propanol, piroliza pentru obținerea metanului și cetenei, condensarea cu 2 moli de fenol în prezența unui catalizator acid pentru obținerea bisfenolului A. În plus, se poate obține hexacloroacetona prin perclorinare, care conduce mai departe prin descompunere la cloroform cu hidroxid de sodiu. [1]
Bibliografie
1. Stylianos Sifinades, A.B.L., Acetone, in Ullmann's Encyclopedia of Industrial Chemistry. 2005, Wiley-VCH: New Jersey.
2. Howard, W.L., Acetone, in Kirk-Othmer Encyclopedia of Chemical Technology, Watcher, Editor. 2000. p. 92-101.
3. SIDS, O., Acetone. 1999, UNEP Publications: USA.
4. http://www.npi.gov.au/resource/acetone. 24.12.2017].
5. Huang, T., Acetone in Chemical Prices. 2017, ICIS: UK.
6. Greiner, C.F., Acetone. Chemical Economics Handbook. 2016: SRI consulting.
Preview document
Conținut arhivă zip
- Procese industriale de obtinere acetona.docx