Extras din referat
Aspecte teoretice
Generalitati asupra spectrelor electronice Lungimi de unda , frecvente , energii
Spectroscopia in domeniul vizibil si ultra violet face parte dintre cele mai vechi metode fizice de investigatie a substantelor organice. Ambele tipuri de spectre ( intre care nu exista nici o diferenta principal) sunt associate cu tranzitiile electronice care au loc atunci cand o molecula trece din starea fundamental intr-o stare excitata. Ca urmare , spectrele corespunzatoare , numite spectre electoronice , vor da informatii aupra starii electronice a moleculelor.
Un spectru electronic reprezinta curba de absorbtie a energiei atunci cand substnta este supusa actinii radiatiilor din domeniile amintite. Abscisa este de obicei gradata in lungimi de unda ( mai rar in frecvente) iar pe ordonata se inscribe un parametru referitor la absorbtie (de obicei Ɛ sau log Ɛ).
De cele mai multe ori in spectrometria in vizibil si ultraviolet lungimile de unda se exprima in mµ sau in angstrmini ( 1mµ = 1nm = 10 Å = 10-7 cm ). Pentru spectrul vizibil , in concordant cu domeniul de sensibilitatea a ochiului omenesc , lungimile de unda sunt cuprinse intre 400 mµ si 800 mµ ( lumina violeta 400 – 435 mµ , albastru 435 – 480 , verde 500 560 mµ , galben mµ , portocaliu 600mµ si rosu 600-700mµ).
Domeniul ultraviolet reprezinta radiatiile cu lungimi de unda mai mici decat 400 mµ pentru care ochiul omenesc nu este sensibil Regiunea cea mai interesanta este cuprinsa intre 180 mµ si 400 mµ , ermitand lucrul in aer , respective azot La lungimi de unda ai mici ( 120 – 180 mµ ) se afla domeniul ultravioletului de vid sau ultravioletul lui Schuman (sub 180 mµ componentele aerului absorb puternic radiatiile)
De multe ori pe abscisa spectrelor este trecuta marimea ῠ (numar de unda ) care reprezinta inversul lungimii de unda si este data de ralatia (1) ( aplicata si in infrarosu).
(1)
Se vede deci ca in domeniul vizibil si ultraviolet , numerele de unda au valori de ordinul 12500 cm-1 ( la λ = 800mµ ) – 50000cm-1 ( la λ = 200mµ ).
Absorbtia unei cuante de lumina ( din domeniul vizibil sau ultraviolet ) de care o molecula produde trecerea acesteia de la energia starii fundamentale (E1) la energia mai mare a starii excitate (E2) Ca urmare , si in cazul tranzactiilor electronice , la absorbtia cuantei va fi satisfacuta cunoscuta relatie (2):
E = E2 – E1 = h - υ = (2) Pentru a determina marimea energiilor cuantelor din acest domeniu se aplica relatia (2) ( modificata cu coeficientii de transformare in unitatile de masura uzuale) :
Astfel , pentru cuantele din domeniul vizibil corespund energii de la 35,7 kcal / mol ( la λ = 800 mµ) pana la 71,5 kcal / mol ( la λ =400 mµ ) , iar pentru cuantele din domeniul ultraviolet valori de 71,5 kcal / mol pana la 159 kcal / mol ( la λ =180mµ) ( in domeniul ultraviletului de vid energiile sunt corespunzator si mai mari)
Definitii :
Cromofor – este o grupa covalenta nesaturata datorita careia are loc absorbtia electronic
Auxocrom – grupa saturate care atasata unui cromofor modifica lungimea de unda si intensitatea maximului de absorbtie
Notiunile de cromofor si auxocrom au aparut inca in teoria lui O. N. Witt (1876) asupra culorii.
Deplasarea batocroma sau deplasarea spre rosu este deplasarea maximului de absorbtie sprelungimi de unda mai mari
Deplasarea hipsocroma sau deplasare spre albastru este deplasarea maximului de absorbtie spre lungimi de unda mai mici
Efect hipercromic – efectul de crestere a intensitatii de absorbtie.
Effect hipocromic – efectul de descrestere a intensitatii de absorbtie
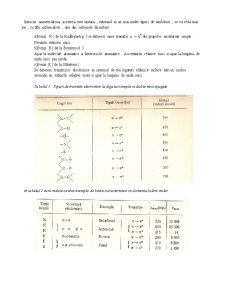
Tipuri de tranzitii electronice :
Tranzitiile electronice ce apar la absorbtia unei cuante din domeniul vizibil si ultraviolet difere dupa natura orbitalului initial si final in care se gasesc electronii implicate in tranzitie.
Orbitalii legaturilor simple , numiti orbital σ , pot fi orbital de legatura σ (ocupati cu electroni in stare fundamental ) si orbital de antilegatura σ* ( neocupati in stare fundamentala , se pot ocupa in stare excitata). In mod analog , orbitalii legaturilor duble orbital π , pot fi si ei de legatura (π) si antilegatura (π*) In afara de acestia , exista orbital de nelegatura , desemnati cu n. Spre deosebire de orbitalii de tip σ sau π , orbitalul n este localizat la un singur atom In fig. 1 sunt reprezentati orbitalii amintiti in ordinea continutului lor energetic si sunt figurate diferitele tranzitii electronice care pot aparea la absorbtia cuantelor din domeniul vizibil si ultraviolet Reprezentarea tipului de tranzactir se face notand tipul orbitalului de la care proneste electronul sic el care ajunge acesta , unind cele doua litere printr-o sageata
Preview document
Conținut arhivă zip
- Spectometria in Ultraviolet si Vizibil - Spectre Vizibile.doc