Extras din referat
1. Legile de baza ale gazelor ideale
Agentul de lucru cel mai utilizat în masinile si instalatiile termice este gazul. Deoarece studiul gazelor reale este complicat a fost conceput un gaz ipotetic numit gaz ideal, definit prin urmatoarele conditii:
- moleculele gazului sunt perfect sferice si perfect elastice;
- volumul propriu al moleculelor este neglijabil în raport cu volumul total ocupat de gaz;
- fortele de interactiune moleculara sunt neglijabile.
Gazele din natura, la presiuni mici si temperaturi mari, se aproprie de gazul ideal, iar legile pentru aceste gaze reale prezinta abateri mici de la legile gazului ideal.
În domeniul de presiuni si temperaturi uzuale pentru functionarea masinilor si instalatiilor termice, gazele tehnice urmeaza legile gazului ideal cu abateri relativ reduse. Datorita acestui fapt au putut fi deduse experimental legile gazelor ideale. Aceste legi nu sunt însa aplicabile vaporilor, care sunt gaze aflate în vecinatatea domeniului lor de lichefiere.
Pentru 2 stari ale gazului, 1 si 2, au fost deduse experimental urmatoarele legi:
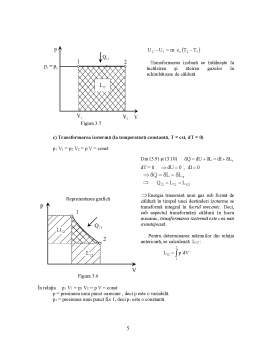
a) Legea Boyle – Mariotte (pentru evolutia izoterma, T = cst)
b) Legea lui Gay – Lussac (pentru evolutia izobara, p = cst)
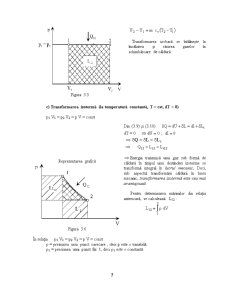
c) Legea lui Charles (pentru evolutie izocora, V = cst)
d) Legea lui Avogadro: Toate gazele ideale care se afla la aceeasi presiune, temperatura si volum contin acelasi numar de molecule.
Kilomolul este o unitate de masura pentru cantitatea de substanta si reprezinta cantitatea de substanta care contine molecule.
nr. lui Avogadro si reprezinta numarul de molecule continute în 12 kg de izotop care are masa moleculara 12.
Masa moleculara a unui gaz este un numar adimensional care arata de câte ori masa unei molecule din gazul respectiv este mai mare decât a 12-a parte din masa moleculei izotopului de carbon .
Masa molara este masa unui kmol de substanta exprimata în kg, care are ca numar tocmai masa moleculara a acestei substante. Se noteaza cu
Ex.: ;
Rezulta relatia pentru masa de substanta (3.1)
unde: m = masa substantei
masa molara
n = nr. kilomoli
Volumul molar, notat = volumul unui kmol de substanta
Din legea lui Avogadro si din definitia pentru kmol, rezulta urmatoarea consecinta: volumul unui kmol de substanta este acelasi pentru toate gazele ideale aflate în conditii egale de presiune si temperatura.
Daca 1 si 2 sunt doua gaze aflate la aceeasi presiune p si temperatura T
(3.2)
În conditii normale fizice volumul unui kmol de gaz, indiferent de natura gazului, are întotdeauna valoarea:
Metrul cub normal.
Pe lânga kilomol si kilogram, ca unitati de masura a cantitatii unei substante, se mai foloseste metrul cub normal cantitatea de gaz cuprinsa în volumul
de 1 m3 în conditii normale fizice.
1 kmol are volumul 22,4 m3, rezulta ca 1 m3N reprezinta a 22,4-a parte dintr-un kmol.
1 kmol = Mi [kg] = 22,4 m3N
2. Ecuatia termica de stare a gazelor ideale
Figura 3.1
Pentru 1 kg de gaz ideal, se considera 1si 2 doua stari oarecare ale gazului.
Indiferent de pozitia punctelor 1 si 2, se poate ajunge din starea 1 în starea 2 printr-o evolutie izoterma 1-x apoi o evolutie izobara x-2.
Preview document
Conținut arhivă zip
- Gaze Ideale.doc